Presentación del caso
Presentación caso clínico: Virginia Rahi1. Discusión: Melisa Realini1. Presentación e informe de necropsia: Luciana Battipiede2, Gabriela Pairola2, Ana Lía Nocito2 Autores: Walter Sacchi1, Francisco Consiglio1, Diego Bértola1, Liliana Negro Marquinez1, Roberto Parodi1, Alcides Greca1. 1Primera Cátedra de Clínica Médica y Terapéutica. Facultad de Ciencias Médicas. Universidad Nacional de Rosario. Servicio de Clínica Médica. Hospital Provincial del Centenario. Rosario. Santa Fe. Argentina. 2Cátedra de anatomía y fisiología patológicas. Facultad de Ciencias Médicas. Universidad Nacional de Rosario. Presentación caso clínico: Virginia Rahi. Residente de 2° año de Clínica Médica.
ENFERMEDAD ACTUAL:
Paciente varón de 40 años de edad, consulta por cuadro de un mes de evolución caracterizado por malestar general y fiebre a predominio nocturna. El cuadro se acompaña de algunos episodios de diarrea no disenteriforme y vómitos alimenticios. Del mismo tiempo de evolución presenta sudoración nocturna y pérdida de peso de aproximadamente 2 kg. Niega otros síntomas acompañantes.
ANTECEDENTES PERSONALES Y FAMILIARES:
Paciente vigil. Impresiona moderadamente enfermo.
Signos vitales: presión arterial: 120/90 mmHg. Frecuencia cardíaca: 136 lpm. Frecuencia respiratoria: 20 rpm. Temperatura: 39,3ºC. Saturación de O2: 99% (aire ambiente).
Cabeza y cuello: normocéfalo, cabello bien implantado. Ojos: conjuntivas pálidas, escleras blancas. Pupilas isocóricas, reactivas y simétricas. Movimientos oculares extrínsecos conservados. Puntos sinusales negativos. Fosas nasales y conductos auditivos externos permeables y sin secreciones. Cavidad bucal: piezas dentarias completas en regular estado, lengua central y móvil, mucosas semihúmedas, orofaringe sin exudados, petequias en paladar. Reflejo nauseoso conservado. Cuello: cilíndrico, simétrico, pulsos carotídeos simétricos, sin soplos, ingurgitación yugular 2/6, con colapso inspiratorio. No se palpan adenopatías cervicales ni supraclaviculares. No se palpa tiroides.
Tórax: diámetro ántero-posterior normal, sin cicatrices. Columna sonora, sin desviaciones, indolora. Múltiples tatuajes.
Aparato cardiovascular: no observo ni palpo latidos patológicos ni frémito. R1 y R2 normofonéticos, sin soplos, R3 ni R4. Ritmo regular.
Aparato respiratorio: respiración costo-abdominal, sin tiraje ni reclutamiento. Expansión de bases y vértices conservados. Vibraciones vocales conservadas. Sonoridad pulmonar conservada. Murmullo vesicular conservado sin ruidos agregados.
Abdomen: plano. Sin cicatrices ni circulación colateral. Blando, depresible, indoloro. Timpanismo conservado. No se palpan visceromegalias. Ruidos hidroaéreos conservados. Puño percusión bilateral negativa.
Examen Neurológico: orientado globalmente. Sin foco motor ni sensitivo. Pares craneales conservados. Sin signos meníngeos. Espinopalpación negativa. Flapping y rueda dentada negativos.
Miembros: tono, trofismo, pulsos y temperatura conservados. Sin edemas ni adenopatías. Homans y Ollow negativos.
Genitales: testículos en bolsas. Escroto sin lesiones. Pene sin lesiones ni secreción por meato uretral.
EXAMENES COMPLEMENTARIOS:
Laboratorio:
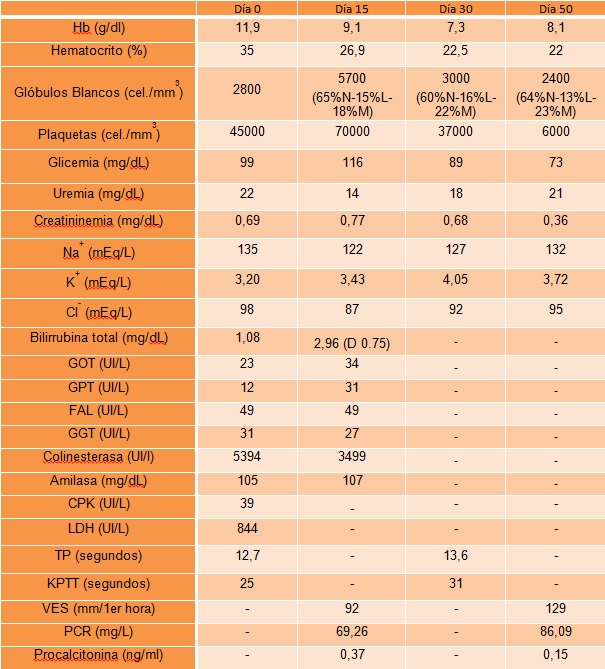 Frotis de sangre periférica:
Frotis de sangre periférica:
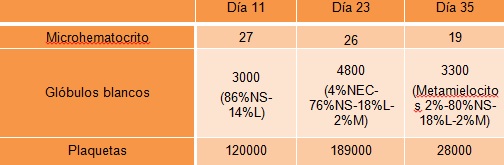
EVOLUCIÓN:
Al ingreso se diagnostica infección por virus de la inmunodeficiencia humana (linfocitos CD4: 8 cél/ul). Se interpreta inicialmente como síndrome febril sin foco claro asociado a pancitopenia por lo que se toman cultivos y se mantiene conducta antibiótica expectante.
Día 10 de internación se inicia tratamiento antirretroviral.
El paciente evolucionó febril persistente con regular estado general. Se realizaron múltiples estudios complementarios: toma de muestras para cultivos (sin aislamientos al ingreso); lavado bronquioalveolar (BAL); punción biopsia de médula ósea (PBMO); examen de líquido cefalorraquídeo sin hallazgos de jerarquía.
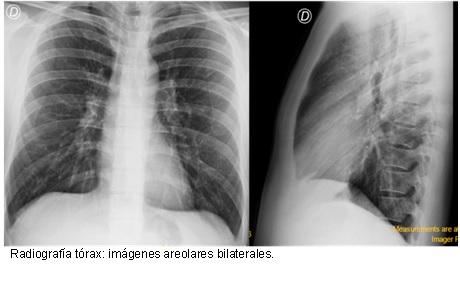
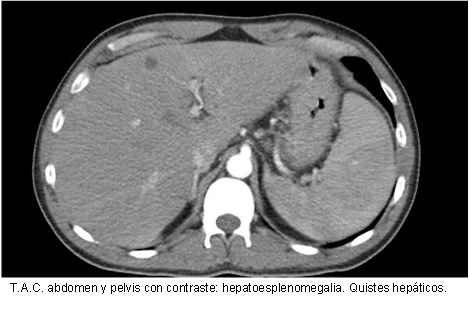
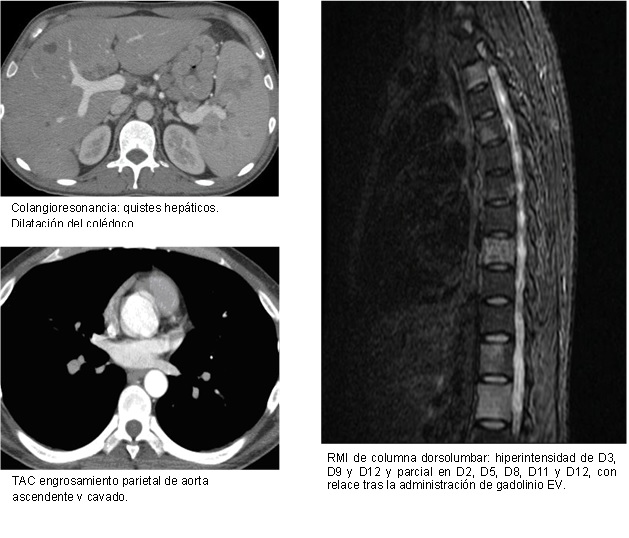
Se realizaron diversos estudios por imágenes: ecografía abdominal que impresiona dilatación del colédoco; tomografía de tórax, abdomen y pelvis con evidencia de hepatoesplenomegalia sin otros hallazgos. Se solicitó Colangio-RMI para mejor evaluación de vía biliar sin alteraciones a dicho nivel pero con hallazgo incidental de lesiones hiperintensas a nivel de columna dorso-lumbar.
Evolucionó febril persistente a pesar de tratamiento antibiótico dirigido (14 días) por lo que por sospecha de complicación supurativa se solicita angio-TAC de tórax y abdomen con signos sugestivos de aortitis a nivel de aorta ascendente. Se toman hemocultivos de control, negativos.
Se repite nueva punción de médula ósea para cultivo, sin aislamientos.
Al día 48 de internación, por persistir sin mejoría en curva febril, se decide cambiar esquema antibiótico a imipenem más trimetorpima-sulfametoxazol.
ANEXO
ENFERMEDAD ACTUAL:
Paciente varón de 40 años de edad, consulta por cuadro de un mes de evolución caracterizado por malestar general y fiebre a predominio nocturna. El cuadro se acompaña de algunos episodios de diarrea no disenteriforme y vómitos alimenticios. Del mismo tiempo de evolución presenta sudoración nocturna y pérdida de peso de aproximadamente 2 kg. Niega otros síntomas acompañantes.
ANTECEDENTES PERSONALES Y FAMILIARES:
- Ex presidiario (privado de la libertad hasta 18 meses previos a la internación).
- Tabaquista y etilista ocasional.
- Consumidor de cocaína inhalatoria.
- Viajes frecuentes a países de América Central
- Padre: fallecido de neoplasia ósea, se desconocen más datos. Madre, hijos y hermanos vivos, sanos.
Paciente vigil. Impresiona moderadamente enfermo.
Signos vitales: presión arterial: 120/90 mmHg. Frecuencia cardíaca: 136 lpm. Frecuencia respiratoria: 20 rpm. Temperatura: 39,3ºC. Saturación de O2: 99% (aire ambiente).
Cabeza y cuello: normocéfalo, cabello bien implantado. Ojos: conjuntivas pálidas, escleras blancas. Pupilas isocóricas, reactivas y simétricas. Movimientos oculares extrínsecos conservados. Puntos sinusales negativos. Fosas nasales y conductos auditivos externos permeables y sin secreciones. Cavidad bucal: piezas dentarias completas en regular estado, lengua central y móvil, mucosas semihúmedas, orofaringe sin exudados, petequias en paladar. Reflejo nauseoso conservado. Cuello: cilíndrico, simétrico, pulsos carotídeos simétricos, sin soplos, ingurgitación yugular 2/6, con colapso inspiratorio. No se palpan adenopatías cervicales ni supraclaviculares. No se palpa tiroides.
Tórax: diámetro ántero-posterior normal, sin cicatrices. Columna sonora, sin desviaciones, indolora. Múltiples tatuajes.
Aparato cardiovascular: no observo ni palpo latidos patológicos ni frémito. R1 y R2 normofonéticos, sin soplos, R3 ni R4. Ritmo regular.
Aparato respiratorio: respiración costo-abdominal, sin tiraje ni reclutamiento. Expansión de bases y vértices conservados. Vibraciones vocales conservadas. Sonoridad pulmonar conservada. Murmullo vesicular conservado sin ruidos agregados.
Abdomen: plano. Sin cicatrices ni circulación colateral. Blando, depresible, indoloro. Timpanismo conservado. No se palpan visceromegalias. Ruidos hidroaéreos conservados. Puño percusión bilateral negativa.
Examen Neurológico: orientado globalmente. Sin foco motor ni sensitivo. Pares craneales conservados. Sin signos meníngeos. Espinopalpación negativa. Flapping y rueda dentada negativos.
Miembros: tono, trofismo, pulsos y temperatura conservados. Sin edemas ni adenopatías. Homans y Ollow negativos.
Genitales: testículos en bolsas. Escroto sin lesiones. Pene sin lesiones ni secreción por meato uretral.
EXAMENES COMPLEMENTARIOS:
Laboratorio:


|
Al ingreso se diagnostica infección por virus de la inmunodeficiencia humana (linfocitos CD4: 8 cél/ul). Se interpreta inicialmente como síndrome febril sin foco claro asociado a pancitopenia por lo que se toman cultivos y se mantiene conducta antibiótica expectante.
Día 10 de internación se inicia tratamiento antirretroviral.
El paciente evolucionó febril persistente con regular estado general. Se realizaron múltiples estudios complementarios: toma de muestras para cultivos (sin aislamientos al ingreso); lavado bronquioalveolar (BAL); punción biopsia de médula ósea (PBMO); examen de líquido cefalorraquídeo sin hallazgos de jerarquía.
Se realizaron diversos estudios por imágenes: ecografía abdominal que impresiona dilatación del colédoco; tomografía de tórax, abdomen y pelvis con evidencia de hepatoesplenomegalia sin otros hallazgos. Se solicitó Colangio-RMI para mejor evaluación de vía biliar sin alteraciones a dicho nivel pero con hallazgo incidental de lesiones hiperintensas a nivel de columna dorso-lumbar.
DETALLES DE EXÁMENES COMPLEMENTARIOS
|
Se completa evaluación con RMI de columna con hallazgo de alteraciones sugestivas de espondilitis. Se realiza punción ósea bajo TAC con toma de cultivos y biopsia.
El día 20 de internación, comenzó con síntomas urinarios y diarrea con aislamiento de Salmonella no typhi en urocultivo y coprocultivo por lo que se inició tratamiento con ciprofloxacina. Se toman nuevos hemocultivos obteniéndose el mismo aislamiento por lo que se agrega al tratamiento previo ceftriaxona.| RMI columna dorsolumbar Los discos intervertebrales visualizados son de altura, morfología e intensidad normal de la señal. No presentan protrusiones ni hernias discales. Los cuerpos vertebrales son de morfología normal. Se observa alteración en la intensidad de la señal a nivel de los cuerpos vertebrales de D3, D9 y D12 y parcial en D2, D5, D8, D11 y D12, siendo hiperintensos en T2 y STIR con relace tras la administración de gadolinio EV. Los cuerpos vertebrales lumbares son de morfología normal. Presentan similar afectación que las vértebras dorsales, con mayor compromiso de L2. Se observa compromiso del sacro, con extensión a ambos ilíacos siendo de mayor jerarquía el izquierdo. Dichos hallazgos son compatibles con procesos inflamatorio- infeccioso de los cuerpos vertebrales. |
Evolucionó febril persistente a pesar de tratamiento antibiótico dirigido (14 días) por lo que por sospecha de complicación supurativa se solicita angio-TAC de tórax y abdomen con signos sugestivos de aortitis a nivel de aorta ascendente. Se toman hemocultivos de control, negativos.
Se repite nueva punción de médula ósea para cultivo, sin aislamientos.
Al día 48 de internación, por persistir sin mejoría en curva febril, se decide cambiar esquema antibiótico a imipenem más trimetorpima-sulfametoxazol.
DETALLES DE EXÁMENES COMPLEMENTARIOS
|
ANEXO



Segunda parte
Discusión: Melisa Realini. Residente de 3° año de Clínica Médica.
¿Qué paciente es el que consulta?
Hay algunas certezas de las que se disponen, estamos ante un paciente con diagnóstico reciente de HIV, con un estado de inmunosupresión severo con muy bajo recuento de linfocitos CD4, con un síndrome febril aparentemente sin respuesta a los tratamientos aplicados a pesar de ser dirigidos a gérmenes específicos.
¿Estamos realmente ante un paciente con Fiebre de origen desconocido (FOD)?
La FOD en el paciente HIV ha sido definida como temperatura mayor a 38,3ºC medida en varias ocasiones en más de 4 semanas en pacientes ambulatorios; o de más de 3 días en pacientes hospitalizados, infectados por VIH, luego de 3 días de estudio apropiado, con un mínimo de 2 días de incubación de los cultivos, que no revela la causa. Si pensamos en este paciente, las causas de fiebre, principalmente infecciosas fueron ampliamente estudiadas y descartadas, siendo las únicas manifestaciones iniciales las gastrointestinales, compatibles por lo menos en el inicio con el aislamiento de Salmonella.
Las manifestaciones gastrointestinales en el paciente HIV están dentro de las más comunes y se encuentran asociadas con aumento de mortalidad. La diarrea ocurre hasta en un 90% de los pacientes con infección por HIV sin tratamiento antirretroviral (ARV) y en un 18% de los casos de HIV constituye la primera manifestación, por lo que es fundamental solicitar serología para HIV en todo paciente que presente diarrea crónica, como el caso estudiado donde dicho cuadro fue la clave para el diagnóstico al ingreso de HIV. La infección por HIV resulta en una depleción rápida del recuento de linfocitos T CD4 en el tracto gastrointestinal, así como la característica enteropatía con aumento de la inflamación de la lámina propia y daño del epitelio gastrointestinal, lo que se asocia con translocación bacteriana y activación inmune.
Los pacientes sin SIDA están predispuestos a infecciones intestinales, que pueden ser desde síndrome diarreico agudo hasta infecciones crónicas intratables por microorganismos que usualmente son autolimitados en individuos inmunocompetentes.
Se debe caracterizar la diarrea interrogando al paciente acerca del volumen, duración y frecuencia así como también los síntomas asociados como náusea, dolor abdominal, sangrado, pérdida de peso, fiebre y otras presentaciones. En este caso hablamos de una diarrea crónica mayor a cuatro semanas y de características compatibles con afectación a nivel de intestino delgado, probablemente inflamatoria.
El listado de causas infecciosas es amplio, y varía la frecuencia de los distintos patógenos dependiendo de la población estudiada. En todos estos estudios es alta la proporción de diarreas con más de un agente patógeno así como la proporción de diarreas sin causa detectada, entre las causas más frecuentes se encuentran las parasitarias (Criptosporidium, Isospora belli y Microsporidium). Entre las etiologías virales de diarrea, el citomegalovirus es de los agentes más comunes y graves, manifestándose principalmente con colitis. Otras causas de diarreas virales son adenovirus, rotavirus y enterovirus.
En cuanto a los agentes bacterianos causantes de diarrea, se encuentran infecciones inespecíficas por Salmonella, Shigella, Campilobacter y Clostridiumy las específicas por micobacterias.
La salmonelosis, la cual presentó el paciente, tiene una incidencia veinte veces mayor en los pacientes con SIDA que en la población general. El mecanismo patógeno se da inicialmente por invasión epitelial de la mucosa gastrointestinal donde produce una gastroenteritis secretora, posteriormente y por penetración de la pared se produce invasión submucosa y afectación ganglionar, desde donde se puede producir la diseminación hematógena y eventualmente la siembra en otras localizaciones.
Puede ser asintomática o presentarse con fiebre, malestar general, mialgias, cefalea, tos, diarrea, constipación, dolor abdominal, hepatomegalia, esplenomegalia, bradicardia, linfadenopatía generalizada, exantema y colecistitis al igual que este paciente. A partir de la diseminación hematógena puede dar complicaciones supurativas por embolias sépticas, afectando las mismas principalmente el lecho vascular (aortitis, endocarditis), óseas, articulares y meníngeas, las cuales deben ser tenidas en cuenta en un paciente que evoluciona febril a pesar del tratamiento antibiótico dirigido.
¿Presentó el paciente un cuadro de aortitis?
La aortitis es una enfermedad caracterizada por la afectación inflamatoria y la alteración estructural de la pared vascular aórtica. Las manifestaciones clínicas de las mismas pueden consistir en aneurismas, disección y ruptura o afectación de la pared vascular sin las modificaciones estructurales antedichas. La infección de la pared aórtica es una entidad poco frecuente. La infección por Salmonella es la causa más habitual de aortitis bacteriana por su tendencia a infectar tejidos lesionados, como el endotelio vascular arterioesclerótico.
Las manifestaciones clínicas son las propias del foco infeccioso primario, añadidas a fiebre persistente. Diversas manifestaciones periféricas pueden estar presentes en estos enfermos: petequias, hemorragias en astilla, nódulos de Osler, lesiones de Janeway en ausencia de endocarditis.
El médico no suele sospechar la aortitis por lo inespecífico de sus síntomas, por lo que las técnicas de imagen son de gran ayuda, siendo en general la TAC la primera elección para evaluar la pared del vaso. Un PET-CT podría ser de utilidad en este caso.
¿Debemos pensar en espondilodiscitis infecciosa ante los hallazgos a nivel de columna?
La infección hematógena es la causa más común de espondilitis. La presentación clínica es inespecífica, lo que condiciona un gran retraso diagnóstico. El dolor dorsal o lumbar es constante pero inespecífico y suele ser de tipo inflamatorio. El dolor a la espinopresión/percusión es posiblemente el signo más fiable. Suele acompañarse de hipomovilidad o posturas antálgicas.
La resonancia magnética es la técnica de imagen más sensible y específica, siendo característico de dichas lesiones la afectación discal y de caras articulares de las vértebras, generalmente de comienzo a nivel anterior de los cuerpos vertebrales, con aumento de la señal de intensidad en T2 asociado a una disminución de la intensidad en T1, dichos hallazgos no son compatibles con la clínica y las imágenes de este paciente.
Entre las causas tumorales, los linfomas, principalmente linfoma no Hodgkin (LNH) y el sarcoma de Kaposi son las neoplasias que más comúnmente se encuentran en el intestino delgado y colon, aunque su forma de presentación no es en general con diarrea.
El sarcoma de Kaposi (SK) es la neoplasia más frecuente asociada a SIDA. Es una neoplasia mesenquimática que se origina en el endotelio vascular y linfático. Es la neoplasia abdominal más frecuente en estos pacientes. Esta enfermedad suele ser asintomática, sin embargo es frecuente la pérdida de peso, el dolor abdominal, los vómitos, la diarrea y el síndrome de malabsorción, también se ha informado sangrado gastrointestinal y obstrucción gástrica, casi todos síntomas compatibles con la clínica del paciente.
Puede además presentarse de forma fulminante con compromiso visceral extenso. En cuanto a los hallazgos endoscópicos pueden ser variados desde lesiones ulceradas que se confunden con úlceras pépticas hasta las lesiones submucosas nodulares, vasculares de color púrpura. Es importante resaltar que no siempre las biopsias endoscópicas son diagnósticas, pues se trata de una lesión submucosa.
¿Es correcto pensar en un SK en un paciente sin lesiones cutáneas?
El SK gastrointestinal puede ser sincrónico o asincrónico con el compromiso cutáneo y entre un 15 - 30% de los pacientes con SK visceral no presenta compromiso cutáneo alguno, por lo que dicho cuadro es compatible con la clínica del paciente y puede ser un diagnóstico probable.
El LNH es el segundo proceso maligno más frecuentemente asociado al VIH. El mismo es dos veces más frecuente en hombres que en mujeres, presentándose en forma extranodal con más frecuencia en pacientes HIV-positivo que pacientes HIV-negativo, siendo el tracto gastrointestinal el sitio extranodal más comúnmente afectado. El linfoma difuso de células grandes B (LDCGB) y el linfoma de Burkitt son las formas más comunes de LNH. Por otro lado, los linfomas de tejido linfoide asociado a mucosas (TLAM) de tipo gástrico son comúnmente asociados a la infección por Helicobacter pylori.
Los síntomas del linfoma gástrico son trastornos dispépticos, plenitud posprandial y saciedad precoz. La progresión de la enfermedad lleva al dolor epigástrico, pérdida de peso y de síntomas originados por el compromiso orificial del cardias o del píloro. La hemorragia, no siempre grave, se asocia con mayor frecuencia con los linfomas de alto grado. Síntomas sistémicos o síntomas B como fiebre, sudoración nocturna, pérdida de peso, malestar general son compatibles con el cuadro clínico del paciente.
La tomografía computada sirve para estadificar el linfoma y para evaluar la progresión o el grado de remisión de la enfermedad, pero las lesiones mucosas frecuentemente no son detectadas; la endoscopía puede mostrar erosiones, úlceras, pliegues engrosados, nódulos, pólipos e infiltración submucosa, siendo necesaria la toma de biopsias múltiples y profundas para llegar al diagnóstico. Las metástasis óseas del linfoma pueden dar imágenes parcheadas a nivel de varias vértebras, en general sin afectar los discos intervertebrales, con aumento de intensidad tanto en T2 como en T1, lo que hace pensar en un diagnóstico probable que justifica el daño vertebral de este paciente.
¿Cuál fue la causa de la profundización de pancitopenia en este paciente?
Las alteraciones hematológicas se encuentran entre las complicaciones más frecuentes del HIV, especialmente en estadios avanzados de la enfermedad siendo causa común de mortalidad en este grupo de pacientes. Son múltiples las causas que pueden afectar la médula ósea, habiendo sido descartadas con múltiples estudios y cultivos las causas infecciosas.
El síndrome hemofagocítico (SHF) es una entidad multicausal con hallazgos clínicos y paraclínicos comunes, caracterizado por afección al estado general, fiebre, hepatoesplenomegalia, falla hepática, pancitopenia, adenopatías y coagulopatía, todo esto acompañado de proliferación de tejido linfohistiocitario y hemofagocitosis. Se caracteriza por la proliferación de macrófagos que fagocitan elementos hematopoyéticos y diferentes linajes celulares sanguíneos maduros.
Existen diferentes condiciones que llevan a que este proceso se desencadene, principalmente autoinmunes e infecciosas. El cuadro clínico comprende manifestaciones inflamatorias sistémicas semejantes a la sepsis, lo que hace fundamental su sospecha y diagnóstico debido a que sus tratamientos difieren completamente. Existen criterios diagnósticos para el mismo (tabla I), cumpliendo el paciente al menos 4 de los 8. Si bien no se puede hacer este diagnóstico, es una causa posible, entre otros factores, de afectación medular en este paciente.
EVOLUCIÓN DEL CASOSe realizan los siguientes estudios complementarios:
Nuevo recuento de linfocitos CD4: 8 cél/ul.
Reacción de Huddleson y rosa de Bengala (día 48): no reactivas.
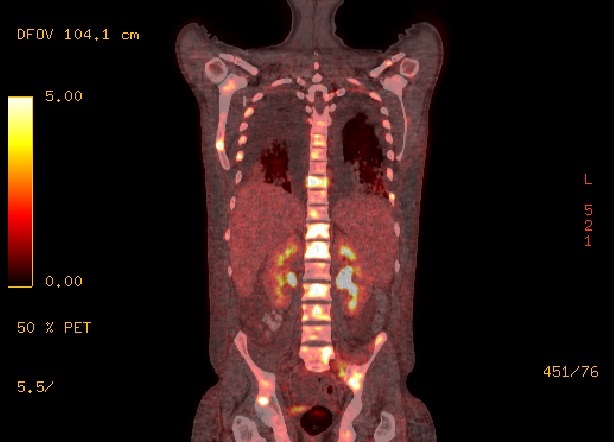
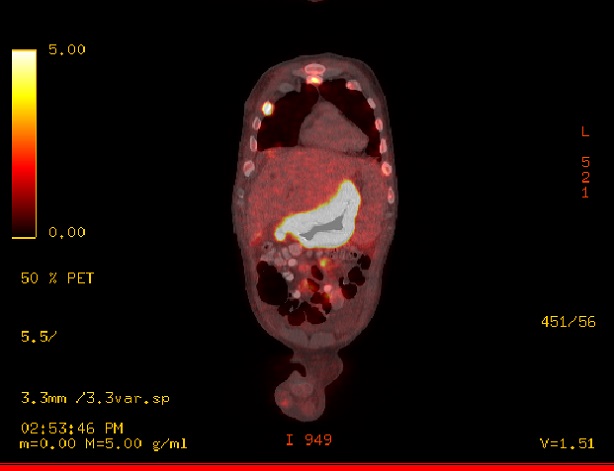
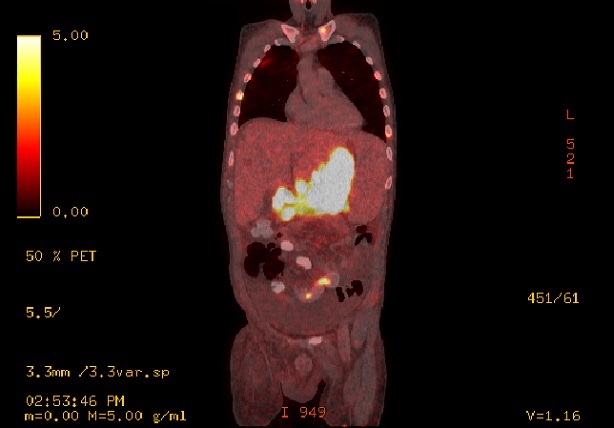
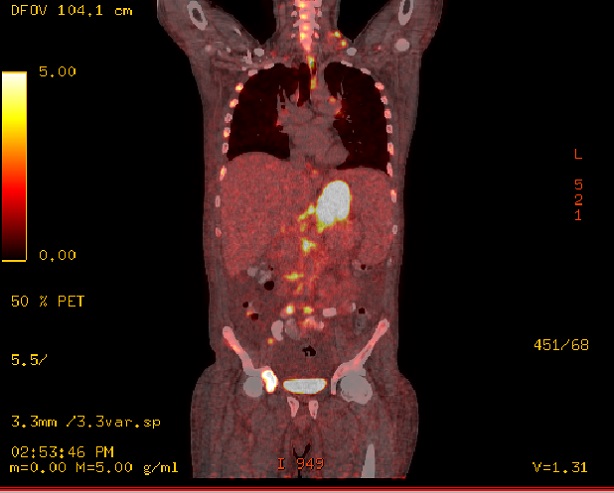
PET/CT Scan (día 48). Hallazgos metabólicos: Aumento difuso del metabolismo gástrico que se asocia a engrosamiento parietal también difuso con un espesor de casi 2 cm, SUV máximo de 21,9. Múltiples adenomegalias hipermetabólicas látero-cervicales, supraclaviculares, mediastínicas, retroperitoneales y mesentéricas, de hasta 16 mm con un SUV máximo de 7,9. Metabolismo óseo aumentado en forma difusa en esqueleto axial con áreas focales de mayor actividad, principalmente en el eje vertebral y huesos de la pelvis. Alteraciones óseas con SUV máximo de 10,2. Hallazgos morfológicos: derrame pleural moderado bilateral con colapso pasivo de segmentos posteriores. Opacidad neumonítica en el lóbulo superior del pulmón derecho en el segmento anterior subpleural, sin definirse lesiones nodulares. Hepatoesplenomegalia y ascitis. Imágenes compatibles con quistes serosos en hígado. Múltiples adenomegalias perigástricas de hasta 2 cm.
El día 51 de internación, habiendo completado 28 días de tratamiento antibiótico, el paciente presenta episodio de hematemesis, insuficiencia respiratoria aguda y shock séptico/hipovolémico, por lo que requiere vinculación a asistencia mecánica respiratoria, administración de noradrenalina e ingreso a unidad de terapia intensiva. En este contexto se agrega vancomicina, anfotericina y tuberculostáticos a su tratamiento.
Se realiza videoendoscopia digestiva alta que evidencia la presencia de candidiasis esofágica, lesiones nodulares y ulceradas en cavidad gástrica, con signos de sangrado reciente.
Posteriormente el paciente evoluciona inestable hemodinámicamente, oligoanúrico, con requerimiento de hemodiálisis y altas dosis de noradrenalina. Fallece al día 54 de internación.
Se realiza necropsia.
*En una semana se publicarán los comentarios finales del caso clínico
Para finalizar, en la evaluación de las causas que llevaron al paciente a la muerte, el mismo ingresa a terapia intensiva con inestabilidad hemodinámica y sangrado digestivo, con claros criterios de shock séptico.
Considero que en el análisis anatomopatológico del estómago va a estar la clave del diagnóstico, siendo probable el hallazgo de células compatibles con linfoma, aunque no es posible descartar otras neoplasias, siendo probablemente lesiones metastásicas a nivel de la columna. En cuanto al estudio de la aorta, considero poco probable el hallazgo de datos patológicos. El estudio de otros órganos como hígado, riñones, intestino delgado podrían presentar signos compatibles con isquemia y congestión propios del cuadro de shock.
INFORME DE NECROPSIA
Luciana Battipiede, Gabriela Pairola, Ana Lía Nocito. Cátedra de Anatomía Patológica.
► Examen externo del cadáver
Se realiza incisión tóraco-abdominal, con extracción del block de vísceras y encéfalo. Se obtienen múltiples cortes representativos de cada órgano.
► Diagnósticos macroscópicos:
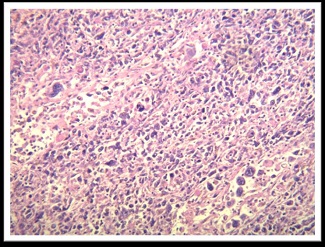
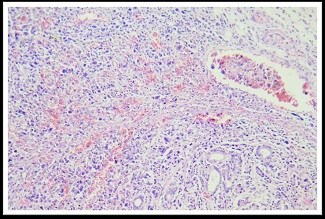
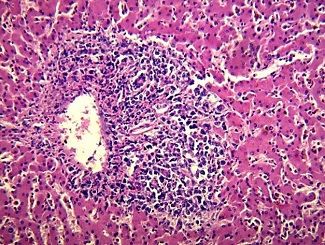
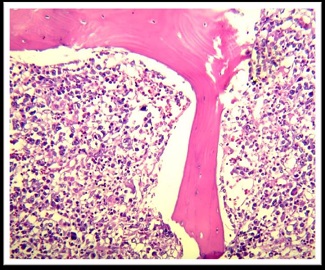
Los cortes representativos evaluados evidencian proceso linfoproliferativo que compromete esófago, estómago, intestino delgado, hígado, bazo, pulmón, hueso y múltiples territorios ganglionares. El mismo se halla integrado por elementos linfoides de gran tamaño, que exhiben núcleos vesiculosos con irregularidad de membrana y nucléolo prominente de localización central, algunos con marcado pleomorfismo, con amplío desarrollo citoplásmatico. Dicho proceso se dispone en patrón difuso, posee además elevado índice mitótico y se acompaña de extensas áreas de hemorragia antigua y reciente. El resto de los órganos de la economía no evidenciaron lesiones. Se solicita estudio inmunohistoquímico: citoqueratina (-), CD20 (-), CD3 (-), antígeno leucocitario común (-), CD30 (+), CD15 (-), PAX 5 (-), KI 67: 80%.
Imágenes del examen histológico de los territorios comprometidos por el proceso linfoproliferativo.
¿Qué paciente es el que consulta?
Hay algunas certezas de las que se disponen, estamos ante un paciente con diagnóstico reciente de HIV, con un estado de inmunosupresión severo con muy bajo recuento de linfocitos CD4, con un síndrome febril aparentemente sin respuesta a los tratamientos aplicados a pesar de ser dirigidos a gérmenes específicos.
¿Estamos realmente ante un paciente con Fiebre de origen desconocido (FOD)?
La FOD en el paciente HIV ha sido definida como temperatura mayor a 38,3ºC medida en varias ocasiones en más de 4 semanas en pacientes ambulatorios; o de más de 3 días en pacientes hospitalizados, infectados por VIH, luego de 3 días de estudio apropiado, con un mínimo de 2 días de incubación de los cultivos, que no revela la causa. Si pensamos en este paciente, las causas de fiebre, principalmente infecciosas fueron ampliamente estudiadas y descartadas, siendo las únicas manifestaciones iniciales las gastrointestinales, compatibles por lo menos en el inicio con el aislamiento de Salmonella.
Las manifestaciones gastrointestinales en el paciente HIV están dentro de las más comunes y se encuentran asociadas con aumento de mortalidad. La diarrea ocurre hasta en un 90% de los pacientes con infección por HIV sin tratamiento antirretroviral (ARV) y en un 18% de los casos de HIV constituye la primera manifestación, por lo que es fundamental solicitar serología para HIV en todo paciente que presente diarrea crónica, como el caso estudiado donde dicho cuadro fue la clave para el diagnóstico al ingreso de HIV. La infección por HIV resulta en una depleción rápida del recuento de linfocitos T CD4 en el tracto gastrointestinal, así como la característica enteropatía con aumento de la inflamación de la lámina propia y daño del epitelio gastrointestinal, lo que se asocia con translocación bacteriana y activación inmune.
Los pacientes sin SIDA están predispuestos a infecciones intestinales, que pueden ser desde síndrome diarreico agudo hasta infecciones crónicas intratables por microorganismos que usualmente son autolimitados en individuos inmunocompetentes.
Se debe caracterizar la diarrea interrogando al paciente acerca del volumen, duración y frecuencia así como también los síntomas asociados como náusea, dolor abdominal, sangrado, pérdida de peso, fiebre y otras presentaciones. En este caso hablamos de una diarrea crónica mayor a cuatro semanas y de características compatibles con afectación a nivel de intestino delgado, probablemente inflamatoria.
El listado de causas infecciosas es amplio, y varía la frecuencia de los distintos patógenos dependiendo de la población estudiada. En todos estos estudios es alta la proporción de diarreas con más de un agente patógeno así como la proporción de diarreas sin causa detectada, entre las causas más frecuentes se encuentran las parasitarias (Criptosporidium, Isospora belli y Microsporidium). Entre las etiologías virales de diarrea, el citomegalovirus es de los agentes más comunes y graves, manifestándose principalmente con colitis. Otras causas de diarreas virales son adenovirus, rotavirus y enterovirus.
En cuanto a los agentes bacterianos causantes de diarrea, se encuentran infecciones inespecíficas por Salmonella, Shigella, Campilobacter y Clostridiumy las específicas por micobacterias.
La salmonelosis, la cual presentó el paciente, tiene una incidencia veinte veces mayor en los pacientes con SIDA que en la población general. El mecanismo patógeno se da inicialmente por invasión epitelial de la mucosa gastrointestinal donde produce una gastroenteritis secretora, posteriormente y por penetración de la pared se produce invasión submucosa y afectación ganglionar, desde donde se puede producir la diseminación hematógena y eventualmente la siembra en otras localizaciones.
Puede ser asintomática o presentarse con fiebre, malestar general, mialgias, cefalea, tos, diarrea, constipación, dolor abdominal, hepatomegalia, esplenomegalia, bradicardia, linfadenopatía generalizada, exantema y colecistitis al igual que este paciente. A partir de la diseminación hematógena puede dar complicaciones supurativas por embolias sépticas, afectando las mismas principalmente el lecho vascular (aortitis, endocarditis), óseas, articulares y meníngeas, las cuales deben ser tenidas en cuenta en un paciente que evoluciona febril a pesar del tratamiento antibiótico dirigido.
¿Presentó el paciente un cuadro de aortitis?
La aortitis es una enfermedad caracterizada por la afectación inflamatoria y la alteración estructural de la pared vascular aórtica. Las manifestaciones clínicas de las mismas pueden consistir en aneurismas, disección y ruptura o afectación de la pared vascular sin las modificaciones estructurales antedichas. La infección de la pared aórtica es una entidad poco frecuente. La infección por Salmonella es la causa más habitual de aortitis bacteriana por su tendencia a infectar tejidos lesionados, como el endotelio vascular arterioesclerótico.
Las manifestaciones clínicas son las propias del foco infeccioso primario, añadidas a fiebre persistente. Diversas manifestaciones periféricas pueden estar presentes en estos enfermos: petequias, hemorragias en astilla, nódulos de Osler, lesiones de Janeway en ausencia de endocarditis.
El médico no suele sospechar la aortitis por lo inespecífico de sus síntomas, por lo que las técnicas de imagen son de gran ayuda, siendo en general la TAC la primera elección para evaluar la pared del vaso. Un PET-CT podría ser de utilidad en este caso.
¿Debemos pensar en espondilodiscitis infecciosa ante los hallazgos a nivel de columna?
La infección hematógena es la causa más común de espondilitis. La presentación clínica es inespecífica, lo que condiciona un gran retraso diagnóstico. El dolor dorsal o lumbar es constante pero inespecífico y suele ser de tipo inflamatorio. El dolor a la espinopresión/percusión es posiblemente el signo más fiable. Suele acompañarse de hipomovilidad o posturas antálgicas.
La resonancia magnética es la técnica de imagen más sensible y específica, siendo característico de dichas lesiones la afectación discal y de caras articulares de las vértebras, generalmente de comienzo a nivel anterior de los cuerpos vertebrales, con aumento de la señal de intensidad en T2 asociado a una disminución de la intensidad en T1, dichos hallazgos no son compatibles con la clínica y las imágenes de este paciente.
Entre las causas tumorales, los linfomas, principalmente linfoma no Hodgkin (LNH) y el sarcoma de Kaposi son las neoplasias que más comúnmente se encuentran en el intestino delgado y colon, aunque su forma de presentación no es en general con diarrea.
El sarcoma de Kaposi (SK) es la neoplasia más frecuente asociada a SIDA. Es una neoplasia mesenquimática que se origina en el endotelio vascular y linfático. Es la neoplasia abdominal más frecuente en estos pacientes. Esta enfermedad suele ser asintomática, sin embargo es frecuente la pérdida de peso, el dolor abdominal, los vómitos, la diarrea y el síndrome de malabsorción, también se ha informado sangrado gastrointestinal y obstrucción gástrica, casi todos síntomas compatibles con la clínica del paciente.
Puede además presentarse de forma fulminante con compromiso visceral extenso. En cuanto a los hallazgos endoscópicos pueden ser variados desde lesiones ulceradas que se confunden con úlceras pépticas hasta las lesiones submucosas nodulares, vasculares de color púrpura. Es importante resaltar que no siempre las biopsias endoscópicas son diagnósticas, pues se trata de una lesión submucosa.
¿Es correcto pensar en un SK en un paciente sin lesiones cutáneas?
El SK gastrointestinal puede ser sincrónico o asincrónico con el compromiso cutáneo y entre un 15 - 30% de los pacientes con SK visceral no presenta compromiso cutáneo alguno, por lo que dicho cuadro es compatible con la clínica del paciente y puede ser un diagnóstico probable.
El LNH es el segundo proceso maligno más frecuentemente asociado al VIH. El mismo es dos veces más frecuente en hombres que en mujeres, presentándose en forma extranodal con más frecuencia en pacientes HIV-positivo que pacientes HIV-negativo, siendo el tracto gastrointestinal el sitio extranodal más comúnmente afectado. El linfoma difuso de células grandes B (LDCGB) y el linfoma de Burkitt son las formas más comunes de LNH. Por otro lado, los linfomas de tejido linfoide asociado a mucosas (TLAM) de tipo gástrico son comúnmente asociados a la infección por Helicobacter pylori.
Los síntomas del linfoma gástrico son trastornos dispépticos, plenitud posprandial y saciedad precoz. La progresión de la enfermedad lleva al dolor epigástrico, pérdida de peso y de síntomas originados por el compromiso orificial del cardias o del píloro. La hemorragia, no siempre grave, se asocia con mayor frecuencia con los linfomas de alto grado. Síntomas sistémicos o síntomas B como fiebre, sudoración nocturna, pérdida de peso, malestar general son compatibles con el cuadro clínico del paciente.
La tomografía computada sirve para estadificar el linfoma y para evaluar la progresión o el grado de remisión de la enfermedad, pero las lesiones mucosas frecuentemente no son detectadas; la endoscopía puede mostrar erosiones, úlceras, pliegues engrosados, nódulos, pólipos e infiltración submucosa, siendo necesaria la toma de biopsias múltiples y profundas para llegar al diagnóstico. Las metástasis óseas del linfoma pueden dar imágenes parcheadas a nivel de varias vértebras, en general sin afectar los discos intervertebrales, con aumento de intensidad tanto en T2 como en T1, lo que hace pensar en un diagnóstico probable que justifica el daño vertebral de este paciente.
¿Cuál fue la causa de la profundización de pancitopenia en este paciente?
Las alteraciones hematológicas se encuentran entre las complicaciones más frecuentes del HIV, especialmente en estadios avanzados de la enfermedad siendo causa común de mortalidad en este grupo de pacientes. Son múltiples las causas que pueden afectar la médula ósea, habiendo sido descartadas con múltiples estudios y cultivos las causas infecciosas.
El síndrome hemofagocítico (SHF) es una entidad multicausal con hallazgos clínicos y paraclínicos comunes, caracterizado por afección al estado general, fiebre, hepatoesplenomegalia, falla hepática, pancitopenia, adenopatías y coagulopatía, todo esto acompañado de proliferación de tejido linfohistiocitario y hemofagocitosis. Se caracteriza por la proliferación de macrófagos que fagocitan elementos hematopoyéticos y diferentes linajes celulares sanguíneos maduros.
Existen diferentes condiciones que llevan a que este proceso se desencadene, principalmente autoinmunes e infecciosas. El cuadro clínico comprende manifestaciones inflamatorias sistémicas semejantes a la sepsis, lo que hace fundamental su sospecha y diagnóstico debido a que sus tratamientos difieren completamente. Existen criterios diagnósticos para el mismo (tabla I), cumpliendo el paciente al menos 4 de los 8. Si bien no se puede hacer este diagnóstico, es una causa posible, entre otros factores, de afectación medular en este paciente.
TABLA I- Criterios diagnósticos del síndrome hemofagocítico
|
|
EVOLUCIÓN DEL CASOSe realizan los siguientes estudios complementarios:
Nuevo recuento de linfocitos CD4: 8 cél/ul.
Reacción de Huddleson y rosa de Bengala (día 48): no reactivas.
PET/CT Scan (día 48). Hallazgos metabólicos: Aumento difuso del metabolismo gástrico que se asocia a engrosamiento parietal también difuso con un espesor de casi 2 cm, SUV máximo de 21,9. Múltiples adenomegalias hipermetabólicas látero-cervicales, supraclaviculares, mediastínicas, retroperitoneales y mesentéricas, de hasta 16 mm con un SUV máximo de 7,9. Metabolismo óseo aumentado en forma difusa en esqueleto axial con áreas focales de mayor actividad, principalmente en el eje vertebral y huesos de la pelvis. Alteraciones óseas con SUV máximo de 10,2. Hallazgos morfológicos: derrame pleural moderado bilateral con colapso pasivo de segmentos posteriores. Opacidad neumonítica en el lóbulo superior del pulmón derecho en el segmento anterior subpleural, sin definirse lesiones nodulares. Hepatoesplenomegalia y ascitis. Imágenes compatibles con quistes serosos en hígado. Múltiples adenomegalias perigástricas de hasta 2 cm.
El día 51 de internación, habiendo completado 28 días de tratamiento antibiótico, el paciente presenta episodio de hematemesis, insuficiencia respiratoria aguda y shock séptico/hipovolémico, por lo que requiere vinculación a asistencia mecánica respiratoria, administración de noradrenalina e ingreso a unidad de terapia intensiva. En este contexto se agrega vancomicina, anfotericina y tuberculostáticos a su tratamiento.
Se realiza videoendoscopia digestiva alta que evidencia la presencia de candidiasis esofágica, lesiones nodulares y ulceradas en cavidad gástrica, con signos de sangrado reciente.
Posteriormente el paciente evoluciona inestable hemodinámicamente, oligoanúrico, con requerimiento de hemodiálisis y altas dosis de noradrenalina. Fallece al día 54 de internación.
Se realiza necropsia.
*En una semana se publicarán los comentarios finales del caso clínico
Imágenes PET




Resolución y anatomía patológica
Discusión final del caso clínico
Opinión de discusora previa a informe de necropsia:Para finalizar, en la evaluación de las causas que llevaron al paciente a la muerte, el mismo ingresa a terapia intensiva con inestabilidad hemodinámica y sangrado digestivo, con claros criterios de shock séptico.
Considero que en el análisis anatomopatológico del estómago va a estar la clave del diagnóstico, siendo probable el hallazgo de células compatibles con linfoma, aunque no es posible descartar otras neoplasias, siendo probablemente lesiones metastásicas a nivel de la columna. En cuanto al estudio de la aorta, considero poco probable el hallazgo de datos patológicos. El estudio de otros órganos como hígado, riñones, intestino delgado podrían presentar signos compatibles con isquemia y congestión propios del cuadro de shock.
INFORME DE NECROPSIA
Luciana Battipiede, Gabriela Pairola, Ana Lía Nocito. Cátedra de Anatomía Patológica.
► Examen externo del cadáver
- Aspecto general: Peso: 85 kg, Talla: 176 cm, Palidez generalizada.
- Cabeza y cuello: Sangre en fosa nasal izquierda.Piezas dentarias en regular estado
- Tórax: Múltiples tatuajes.
- Abdomen: Globuloso. Distendido
- Miembros: Hematoma en pliegue de codo derecho y en ambas muñecas. Múltiples sitios de venopunción antebraquial bilaterales. Tatuajes en ambos miembros superiores. Acceso femoral izquierdo con signos de sangrado reciente. Edema godet +++ infrapatelar.
- Genitales: Ambos testículos en bolsa. Edema escrotal leve a moderado.
Se realiza incisión tóraco-abdominal, con extracción del block de vísceras y encéfalo. Se obtienen múltiples cortes representativos de cada órgano.
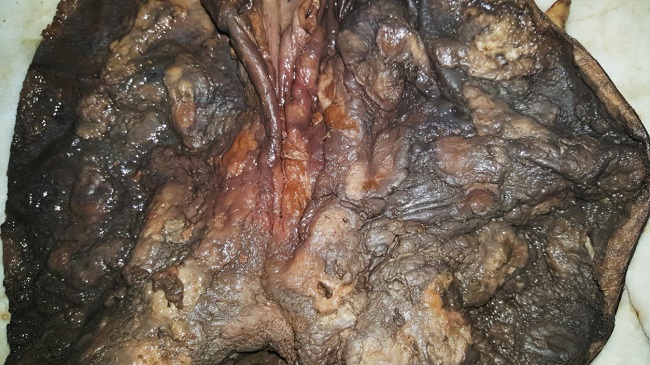
► Diagnósticos macroscópicos:
- Palidez mucocutánea generalizada. Edema en miembros inferiores (+++).
- Hemorragia gástrica alta, masiva, asociada a lesiones nodulares múltiples. Poliadenopatías de predominio perigástrico y peripancreático. Nódulo esofágico de 1 cm. Poliposis intestinal. Hepatomegalia. Esplenomegalia.
- Riñones de shock.
- Derrame pleural de 1000 ml serohemático bilateral. Adherencias pleuropulmonares apicales bilaterales.
- Ateromatosis difusa sin complicaciones.
Los cortes representativos evaluados evidencian proceso linfoproliferativo que compromete esófago, estómago, intestino delgado, hígado, bazo, pulmón, hueso y múltiples territorios ganglionares. El mismo se halla integrado por elementos linfoides de gran tamaño, que exhiben núcleos vesiculosos con irregularidad de membrana y nucléolo prominente de localización central, algunos con marcado pleomorfismo, con amplío desarrollo citoplásmatico. Dicho proceso se dispone en patrón difuso, posee además elevado índice mitótico y se acompaña de extensas áreas de hemorragia antigua y reciente. El resto de los órganos de la economía no evidenciaron lesiones. Se solicita estudio inmunohistoquímico: citoqueratina (-), CD20 (-), CD3 (-), antígeno leucocitario común (-), CD30 (+), CD15 (-), PAX 5 (-), KI 67: 80%.
► Diagnósticos anatomopatológicos finales:
|

Lesiones gástricas / Lesión esofágica
 | 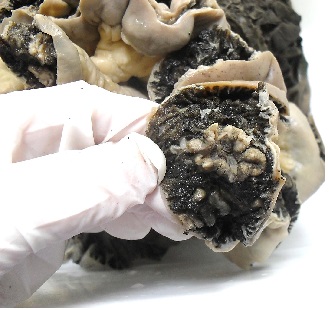 |
Lesiones intestinales
 |  |
 |  |