Autor/a: Oyvind Bruserud, Knut Anders Mosevoll, Einar Kristoffersen, Reidar Kvale, Hakon Reikvam Tidsskr Nor Laegeforen 2021 Jan 11;141(1)
| Introducción |
La trombocitopenia se define como un recuento de plaquetas de < 150 × 109/L y ocurre con frecuencia en los enfermos críticos.
La condición surge como resultado de la reducción de la producción o el aumento de la destrucción o el consumo de plaquetas.
La trombocitopenia en pacientes críticamente enfermos a menudo es consecuencia de múltiples mecanismos fisiopatológicos. Estos deben identificarse si se quiere determinar el pronóstico y proporcionar el tratamiento adecuado.
Este artículo proporciona una descripción general de la trombocitopenia en pacientes críticos, incluidos sus mecanismos fisiopatológicos, curso, evaluación y tratamiento. El trabajo se basa en la literatura identificada a través de una búsqueda no sistemática de la base de datos PubMed y la propia experiencia clínica de los autores.
| Prevalencia y definición |
En un estudio clínico reciente de pacientes en cuidados intensivos y unidades de observación, la trombocitopenia se definió como leve (100-149 × 109/L), moderada (51-99 × 109/L) o grave (<50 × 109/L), con incidencias reportadas de 15.3 %, 5.1 % y 1.6 %, respectivamente. La incidencia de trombocitopenia de nueva aparición entre los pacientes de cuidados intensivos varía del 14 % al 44 %. Más de la mitad de los que pasan más de dos semanas en cuidados intensivos desarrollan trombocitopenia, que se asocia con una alta mortalidad.
| Mecanismos fisiopatológicos |
Las plaquetas se producen en la médula ósea a partir de los megacariocitos, tienen una vida útil de 8 a 10 días y se destruyen principalmente en el bazo. Son esenciales para la hemostasia y también contribuyen a la angiogénesis y la inmunidad innata.
Las causas de la trombocitopenia se pueden dividir en tres categorías principales: reducción de la producción, aumento de la destrucción y aumento del consumo de plaquetas. Un solo paciente a menudo puede exhibir más de uno de estos mecanismos fisiopatológicos simultáneamente (Figura 1). La disfunción plaquetaria es relativamente común en pacientes en estado crítico y puede deberse a uremia, insuficiencia hepática o el uso de medicamentos o una máquina de circulación extracorpórea.
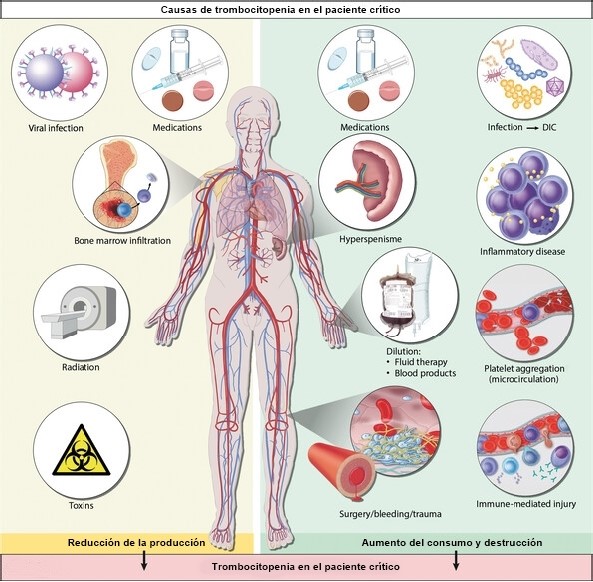
Figura 1. La trombocitopenia es común en pacientes en estado crítico y, a menudo, es el resultado de varios mecanismos fisiopatológicos diferentes. Las causas se pueden dividir en tres categorías principales: reducción de la producción de plaquetas (enfermedad de la médula ósea, uso de quimioterapia o radioterapia, infecciones virales agudas y crónicas, y envenenamientos); aumento del consumo de plaquetas (activación fisiológica de plaquetas durante cirugía/traumatismo/sangrado, activación patológica de plaquetas como en casos de coagulación intravascular diseminada (CID), que con mayor frecuencia se desencadena por infección grave/sepsis) y mayor destrucción de plaquetas (hiperesplenismo, reacciones de hipersensibilidad al fármaco mediadas inmunológicamente y formación de autoanticuerpos, enfermedades inflamatorias, como la linfohistiocitosis hemofagocítica y la agregación plaquetaria en la microcirculación, como en los casos de microangiopatía trombótica). Además, puede producirse trombocitopenia como resultado de un efecto de dilución tras una transfusión masiva de líquidos o hemoderivados.
> Reducción de la producción
No está claro en qué medida la reducción de la producción de plaquetas contribuye a la trombocitopenia en pacientes en estado crítico. Los individuos que se han sometido a quimioterapia citotóxica muestran una producción reducida, al igual que aquellos con enfermedad de la médula ósea o toxicidad aguda por alcohol. Tanto las infecciones virales agudas como crónicas, incluida la hepatitis C, el citomegalovirus, el virus de Epstein-Barr y el parvovirus B19, pueden inhibir la producción de plaquetas. También se ha descrito trombocitopenia en pacientes con COVID-19 grave.
> Aumento del consumo
Las plaquetas pueden ser activadas por los leucocitos, el sistema del complemento, los factores de coagulación, microorganismos y el daño tisular. También juegan un papel clave en la respuesta inmune. La activación de plaquetas mediada por trombina puede ser fisiológica, por ejemplo, en respuesta a cirugía mayor, trauma o pérdida de sangre. La activación patológica de las plaquetas se produce en casos de coagulación intravascular diseminada (CID), que puede desencadenarse por ejemplo, por sepsis o malignidad. Las plaquetas activadas se eliminan rápidamente de la circulación, resultando en trombocitopenia. Los pacientes que reciben tratamiento con oxigenación por membrana extracorpórea también muestran un mayor consumo de plaquetas.
> Mayor destrucción
Más del 50 % de los casos de trombocitopenia en pacientes críticos son el resultado de sepsis o infección grave.
Se ha descrito que tanto los fármacos antiplaquetarios como los antibióticos causan reacciones adversas mediadas por el sistema inmunitario que pueden provocar trombocitopenia. En conjunto, representan alrededor del 15 % de los casos en las unidades de cuidados intensivos. La formación de anticuerpos también puede provocar trombocitopenia.
El ejemplo más común de esto es la formación de anticuerpos contra el complejo heparina-factor plaquetario 4 (PF4); estos anticuerpos causan trombocitopenia inducida por heparina (TIH) cuando las heparinas se utilizan como anticoagulantes. Sin embargo, esto es relativamente raro y se notifica en < 5 % de los pacientes con trombocitopenia en unidades de cuidados intensivos.
| Valoración, diagnóstico y evolución clínica |
La causa subyacente de la trombocitopenia a menudo se puede identificar realizando un historial médico completo y monitoreando el curso clínico, y realizando pruebas de diagnóstico de laboratorio específicas. En alrededor del 25 % de los pacientes en estado crítico con trombocitopenia, la afección tiene más de una causa subyacente (Figura 1).
Es esencial obtener una visión general del historial médico del paciente, las comorbilidades y los medicamentos y luego ver el estado clínico actual a la luz de esta información. Se debe tratar de determinar si la trombocitopenia es el resultado de la enfermedad crítica actual y la disfunción orgánica asociada, o si es parte de una condición subyacente preexistente, como una enfermedad hematológica maligna grave.
También se debe considerar el recuento absoluto de plaquetas, junto con el desarrollo y curso de la trombocitopenia. A menudo se harán evidentes patrones específicos que pueden revelar la causa subyacente (Tabla 1). En general, la trombocitopenia será más grave (< 50 x 109/L) si una causa subyacente crónica se acompaña de factores etiológicos adicionales de nueva aparición; la transfusión de plaquetas puede entonces no lograr aumentar el recuento de plaquetas. Debido al alto recambio de plaquetas, es probable que los recuentos bajos en casos de enfermedad crítica presenten un riesgo hemostático menor que la trombocitopenia causada por insuficiencia de la médula ósea.
También es importante conocer otros factores que pueden contribuir a un recuento bajo de plaquetas. Los ejemplos incluyen pseudotrombocitopenia debido a la agregación de plaquetas inducida por EDTA, hemodilución debido a la infusión de líquidos, transfusiones masivas de otros componentes sanguíneos sin plaquetas o acumulación de plaquetas en el bazo en casos de esplenomegalia o enfermedad hepática con hipertensión portal. Los pacientes con trombocitopenia que desarrollan enfermedad tromboembólica deben someterse a pruebas de condiciones procoagulantes.
| Curso clínico | Causa probable |
| Recuento de plaquetas bajo y sigue siendo bajo | Insuficiencia de la médula ósea Hiperesplenismo |
| El recuento de plaquetas disminuye rápidamente, pero luego se normaliza rápidamente | Cirugía Uso de máquina de circulación extracorpórea Transfusiones masivas sin plaquetas |
| Disminución gradual y normalización del recuento de plaquetas a medida que mejora el estado clínico | Septicemia Pancreatitis Condiciones inflamatorias |
| El recuento de plaquetas desciende y se mantiene bajo a pesar de la mejoría clínica del paciente | Trombocitopenia inducida por fármacos |
| El recuento de plaquetas cae y permanece bajo en pacientes con insuficiencia orgánica persistente | Septicemia Coagulación intravascular diseminada (CID) Insuficiencia circulatoria |
Tabla 1. Cursos clínicos típicos de trombocitopenia en pacientes críticos y posibles causas subyacentes.
| Tratamiento |
En pacientes críticos, la trombocitopenia o una caída rápida en el recuento de plaquetas son marcadores de mal pronóstico y un mayor riesgo de mortalidad.
La condición subyacente del paciente debe ser tratada. Se debe priorizar el control de infecciones y la terapia de soporte de órganos si la trombocitopenia es causada por sepsis, mientras que la hemostasia y las transfusiones de sangre son apropiadas si la trombocitopenia es el resultado de una hemorragia masiva.
Proporcionar el tratamiento correcto depende de la identificación de las causas. La transfusión de plaquetas puede ser el enfoque correcto en pacientes con condiciones que reducen la producción o aumentan el consumo/destrucción de plaquetas, pero puede ser potencialmente dañina en condiciones donde hay una mayor activación intravascular, como trombocitopenia inducida por heparina, púrpura trombocitopénica trombótica o coagulación intravascular diseminada protrombótica.
La transfusión de plaquetas también puede aumentar el riesgo de infecciones nosocomiales y lesiones pulmonares (agudas) relacionadas con la transfusión.
Estos factores justifican un enfoque conservador para el uso de transfusiones de plaquetas, con más énfasis en el tratamiento de la afección subyacente.
>Transfusión terapéutica
Para evitar la trombocitopenia severa y la hemodilución de los factores de coagulación, el sangrado severo debe tratarse con una transfusión balanceada de glóbulos rojos, plasma y plaquetas. De acuerdo con las guías internacionales, se debe considerar la transfusión de plaquetas para pacientes en estado crítico con sangrado y un recuento de plaquetas < 50 x 109/L, o en quienes se sospecha/confirma función plaquetaria reducida.
>Transfusión profiláctica
La razón más común para administrar transfusiones de plaquetas a pacientes en estado crítico es prevenir el sangrado.
La práctica clínica varía considerablemente, pero las guías internacionales recomiendan la transfusión de plaquetas si el recuento es < 10 x 109/L. Se estima que la transfusión aumenta el recuento de plaquetas en alrededor de 15 x 109/L por unidad de transfusión, aunque esto puede variar en un grado relativamente grande.
>Transfusión relacionada a procedimientos
Se recomienda la transfusión de plaquetas para minimizar el riesgo de sangrado durante ciertos procedimientos, por ejemplo, durante la implantación de un catéter venoso central en pacientes con un recuento de plaquetas de < 20 x 109/L. Asimismo, existen guías y recomendaciones para el recuento absoluto de plaquetas en pacientes sometidos a punción lumbar o anestesia epidural (> 50 x 109/L), cirugía mayor (> 50 x 109/L) o neurocirugía (> 100 x 109/L). Sin embargo, estas recomendaciones se basan en gran medida en la experiencia clínica y la base de evidencia es limitada.
> Otras modades de tratamiento
Las drogas pueden afectar la producción y destrucción de plaquetas. En el enfermo crítico, se pueden administrar esteroides si se sospecha que un recuento bajo de plaquetas tiene un origen inmunológico.
Conclusiones
|