1º Parte: Presentación del caso
Este caso clínico será presentado en 3 entregas semanales para abrir espacio al debate en el sector COMENTARIOS.
Enfermedad actual:
Varón de 58 años, consulta por cuadro de 1 mes de evolución caracterizado por dolor abdominal epigástrico de tipo continuo, con exacerbaciones cólicas, e irradiación difusa con predominio en hipocondrio derecho, de aparición postprandial, que aumenta insidiosamente de intensidad 7/10. Se acompaña de distensión abdominal progresiva, náuseas, hiporexia, saciedad precoz y pérdida de peso (10 kg aproximadamente) del mismo tiempo de evolución.
Antecedentes personales:
• Hipertensión arterial diagnosticada hace 2 años en tratamiento con enalapril 10 mg/día.
• Apendicectomía 3 años previos.
• Fractura de arcada cigomática izquierda hace 4 años como consecuencia a un accidente en la vía pública. Como secuela presenta midriasis ocular izquierda, hiporreactiva.
• Hábitos:
- Consumo ocasional de alcohol.
- Niega tabaquismo y consumo de drogas.
Antecedentes familiares:
• Padre: Fallecido. Cirrosis alcohólica.
• Madre: Viva. Colecistectomizada.
• 6 Hermanos: Vivos. Hipertensos.
• 2 Hijos: Sanos.
Examen físico:
Impresiona moderadamente enfermo. Paciente vigil, orientado en tiempo, espacio y persona. Decúbito indiferente.
Signos vitales:
PA: 140/80 mmHg,
FC: 92 lpm,
FR: 18 rpm,
Tº: 36.1 ºC.
Sat: 96% (FiO2 0,21%).
Talla: 1,63 m. Peso: 65 kg.
Piel y faneras: Palidez cutáneo mucosa generalizada.
Cabeza y cuello: Normocéfalo, cabello bien implantado. Conjuntivas rosadas, escleras blancas. Pupilas hiporreactivas, con midriasis izquierda. Movimientos oculares extrínsecos completos. Agudeza visual conservada. Campo visual por confrontación conservado. Puntos sinusales negativos. Fosas nasales permeables sin secreciones. Conducto auditivo externo permeable, sin secreciones ni otorragia. Trago negativo. Cavidad oral con piezas dentarias incompletas y prótesis dentaria, en regular estado. Lengua central y móvil. Orofaringe rosada, sin lesiones. Mucosas semihúmedas. Ganglios submaxilares palpables, no megálicos, indoloros. Cuello cilíndrico, simétrico. Adenopatías cervicales anteriores superiores palpables e indoloras. No palpo tiroides. Ingurgitación yugular 2/6 con colapso inspiratorio completo. Pulsos carotídeos simétricos, sin soplos.
Tórax: Diámetro antero-posterior conservado, sin cicatrices. Columna sonora, sin desviaciones, indolora.
Ap. cardiovascular: No observo latidos patológicos. No palpo frémito. R1-R2 normofonéticos. Ritmo regular. No ausculto soplos ni R3-R4.
Ap. Respiratorio: Respiración costo-abdominal, sin tiraje ni reclutamiento. Expansión de bases y vértices conservada. Vibraciones vocales conservadas. Sonoridad conservada, excursión de bases conservada. Murmullo vesicular disminuidos en ambas bases.
Abdomen: Levemente distendido. Blando, depresible, levemente doloroso a la palpación profunda con predominio en fosa ilíaca izquierda, sin defensa ni descompresión. No palpo hígado ni bazo. Timpanismo conservado. Matidez en flancos desplazable. Ruidos hidroaéreos aumentados. No ausculto soplo. Puñopercusión bilateral negativa.
Neurológico: Funciones superiores conservadas. Sin signos meníngeos. Pares craneales conservados. Sensibilidad y motilidad conservadas. Reflejos osteotendinosos simétricos. Marcha y equilibrio conservados. Respuesta plantar flexora bilateral. Sin flapping ni rueda dentada.
Miembros: Tono, fuerza, trofismo y temperatura conservados. Pulsos distales conservados. Edema Godet + inframaleolar bilateral. Signos de Homans y Ollow negativos.
Examen genital: Pene sin lesiones ni secreciones. Testículos en bolsa. Se palpa a nivel testicular izquierdo superficie irregular e induración en polo inferior indolora.
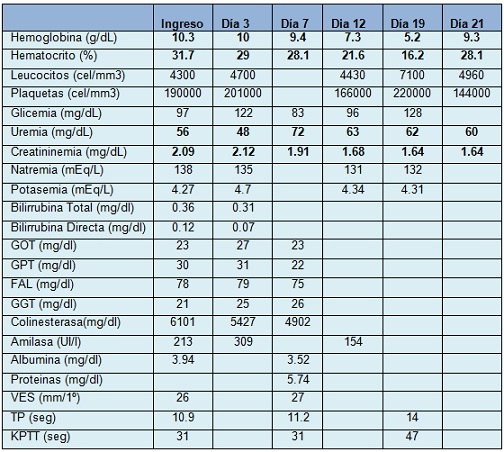
Examenes complementarios al ingreso:
Laboratorio de ingreso
Ritmo sinusal,
regular.
FC: 75 lpm.
PR: 0.16 seg.
QRS: 0.08 seg.
QT 0.32 seg.
AQRS + 20°.
Orina completa:
Amarilla
Límpida
pH:5
Densidad: 1014 – 6
leucocitos/cpo – 2 células epiteliales / cpo.
Índices urinarios: Sodio: 64 mEq/L. Potasio: 40 mEq/L. Cloro: 57.6 mEq/L. Urea: 1846.7 mg/dL. Creatinina: 153.47 mg/dL. .
Perfil lipídico:
Colesterol total: 142 mg/dL.
HDL: 48 mg/dL.
LDL: 78 mg/dL.
Triglicéridos: 82 mg/dL.
Serologías:
HIV-VHB-VHC : no reactivas.
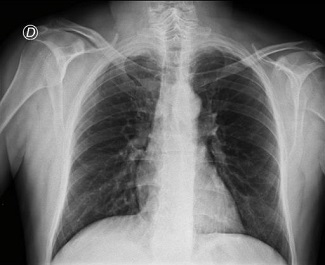
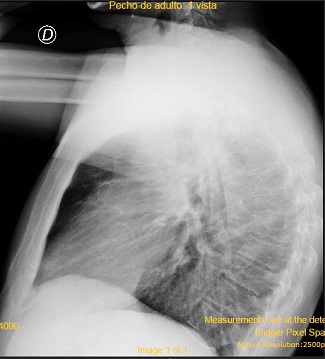
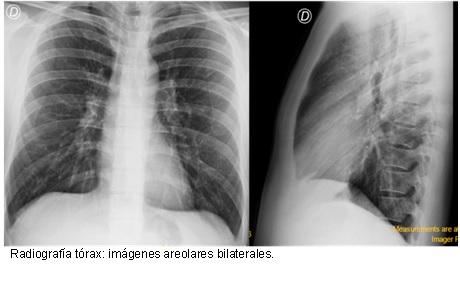
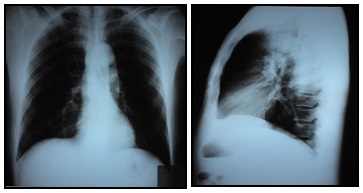
Radiografía de tórax frente y perfil: Índice cardiotorácico conservado.
Sin infiltrados pleuroparenquimatosos.
Fondos de sacos costofrénicos libres. (Imagen 1 y 2).
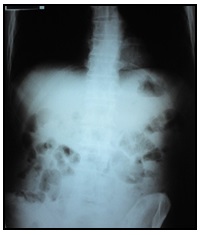
Radiografía de abdomen: Radiopacidad generalizada. Marco colónico dilatado. Impresiona nivel hidroáereo en proyección del ángulo esplénico del colon. (Imagen 3)
Ecografía abdominal (Día 1): Hígado de forma y ecoestructura conservada, tamaño normal. Sin lesiones netas. Vesícula completamente ocupada por contenido ecogénico que no modifica características con cambios posicionales. Vía Biliar con calibre conservado. Páncreas de contorno irregular. Se observa cuerpo y cola con tamaño aumentado. Conducto de Wirsung de 4 mm. Bazo sin esplenomegalia. Riñones: ambos con ecogenicidad aumentada y con moderada dilatación pielocalicial. Moderada cantidad de líquido en cavidad abdominal.
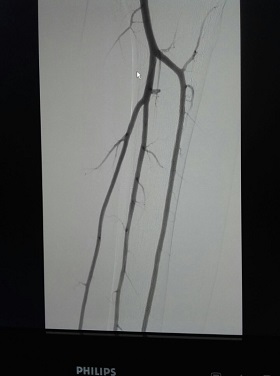
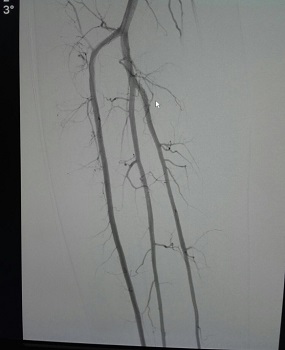
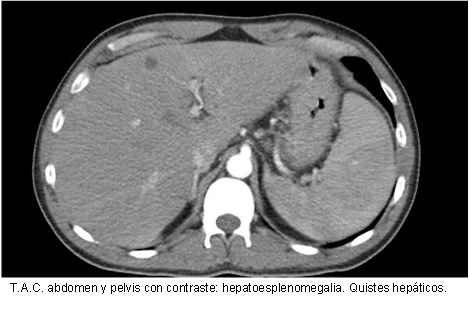
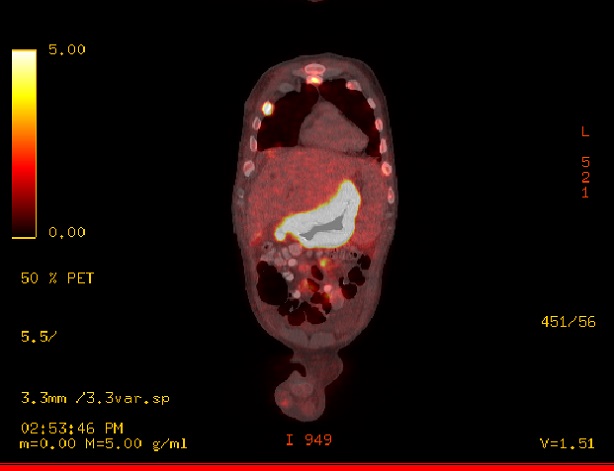
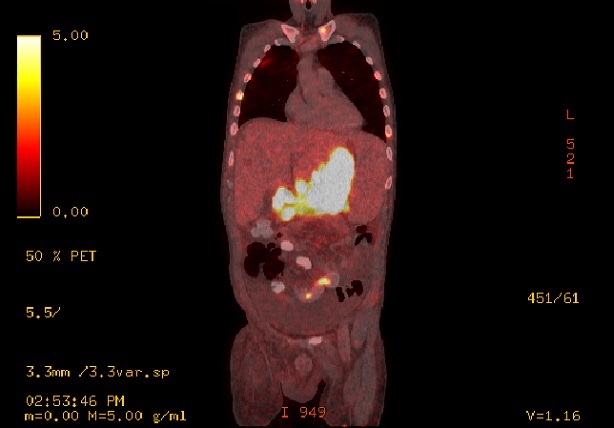
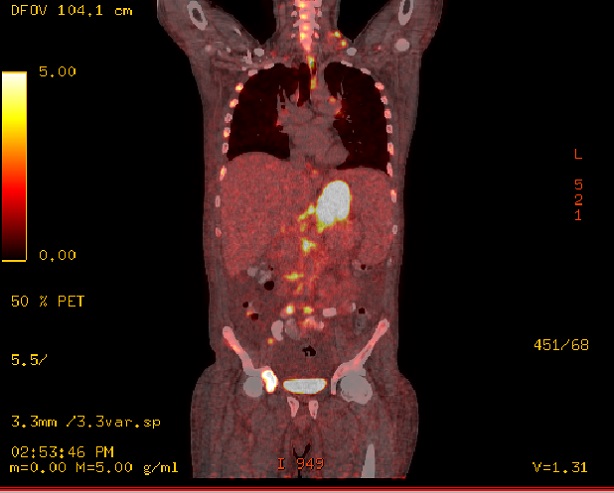
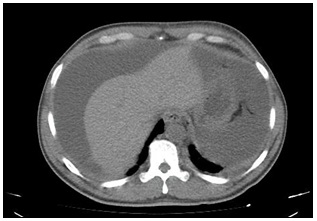
TAC de abdomen y pelvis con contraste (Día 2): Abundante ascitis con extensión hacia la transcavidad de los epiplones. Hígado de pequeño tamaño siendo de forma, tamaño y situaciones habituales, con discreto trastorno perfusional post contraste endovenoso (Imagen 4). Se observa ausencia de flujo en la vena porta a nivel de su segmento inicial, con imagen de defecto de relleno central, con característica de trombosis crónica, identificándose en su topografía la presencia de estructuras vasculares con repermeabilización de la misma a nivel proximal, observándose además trombosis de la vena mesentérica superior y de la vena esplénica, con flujo laminar periférico excéntrico.
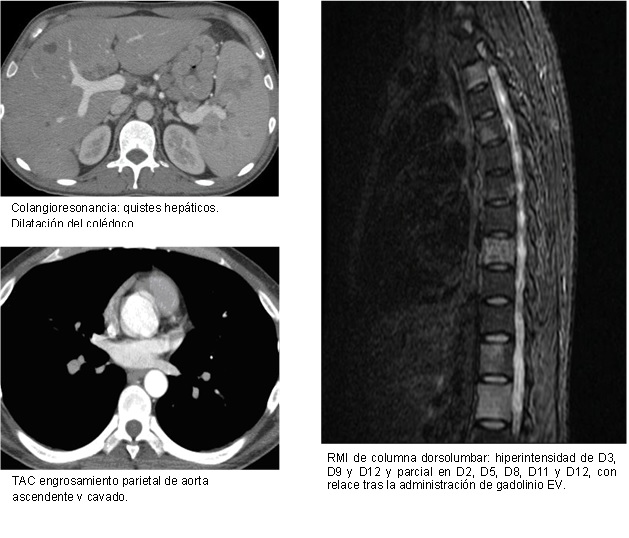
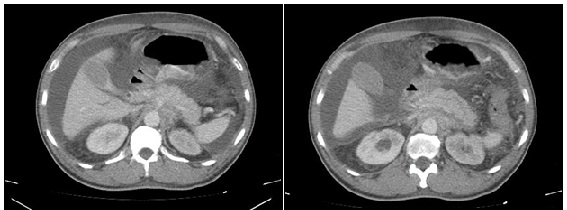
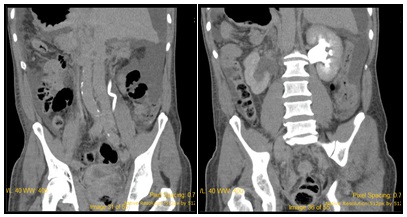
Esto se acompaña de presencia de un tejido de aspecto infiltrativo, sólido, hipovascular, a nivel retroperitoneal, que engloba a la glándula adrenal izquierda y contacte con la curvatura mayor gástrica, determinando un discreto engrosamiento parietal, contacta con la crura diafragmática izquierda, engloba al tronco celíaco y la arteria mesentérica superior, comprime y desplaza el cuerpo pancreático en el sentido anterior (Imágenes 5 y 6), asociado a discreto aumento de la densidad grasa del espacio pararrenal anterior que se acompaña además de dilatación de la vía excretora proximal, sin lograr demostrarse compromiso por infiltración de los uréteres. Se observa un franco retardo de la excreción por medio del contraste renal bilateral lo cual sugiere la afectación funcional de los mismos (Imágenes 7 y 8).
Franco retardo en la eliminación del contraste en la vía de excretora izquierda. Se identifica además un engrosamiento parietal a nivel de la vejiga, en localización posterior y lateral izquierda, de aspecto regular, hipovascular, con un espesor parietal máximo de 16 mm, asociado a una alteración de la grasa paravesical izquierda. Páncreas de características normales. Wirsung de calibre conservado. Edema parietal submucoso a nivel del estómago, fundamentalmente en la región antral, identificándose además una imagen de aspecto tabicada quística, adyacente al ciego, que se interpreta como una adherencia. Prostata y vesículas seminales normales.
Citofisicoquímico de líquido ascítico (día 3):
Amarillento, levemente opalescente.
Glucosa: 1.16 g/L. Proteínas: 1.46 g/L. Albúmina: 1.14 g/L. Colesterol total: 24 mg/dL. TGD: 23 mg/dL. Ácido úrico: 4.7 mg/dL. Colinesterasa: 919 UI/L. Amilasa: 156 UI/L. LDH: 114 UI/L. Bilirrubina total: 0.07 mg/dL. Bilirrubina indirecta: 0.01 mg/dL. pH 7.51. Reacción de Rivalta: +. Elementos 76/mm3.
Cultivo de líquido ascítico (día 3): sin aislamiento microbiológico.
Citología de líquido ascítico (día 3): negativo para células neoplásicas.
Marcadores tumorales (dia 4):- CA 19.9: 3.5 U/ml (0.6- 39 U/ml)
- AFP (Alfafetoproteína): 3.8 ng/ml (0.7- 7.1 ng/ml)
- Sub β- GCH (Subunidad Beta de la Gonadotrofina Coriónica Humana): menor 1 mUI/ml.
Ecografía testicular (día 6): Testículo izquierdo: forma, tamaño y contornos conservados. Parénquima homogéneo. Epidídimo de características ecográficas conservadas. No se observa varicocele ni hidrocele. Se observa moderado varicocele. Testículo derecho: Presenta forma, tamaño y contornos conservados. Parénquima homogéneo. Epidídimo engrosado ecogénico con dos colecciones líquidas, anecoicas, de 7 y 5 mm.
Ecografía renovesical (día 6) : Ambos riñones con situación, tamaño y morfología normal. Sin imágenes de ltiasis. Moderada ectasia pielocalicial bilateral sin disminución del espesor cortical.
2º Parte: Evolución
Tras el hallazgo tomográfico de trombosis en la vena porta, mesentérica superior y esplénica se indica anticoagulación con enoxaparina.
Al descartarse proceso infeccioso asociado y sin evidencias de otra causa identificable del cuadro abdominal se comienza tratamiento con Prednisona 1 mg/Kg por diagnóstico presuntivo de fibrosis retroperitoneal.
El 12do día de internación presenta episodios de melena con caída del hematocrito. Se realiza transfusión de glóbulos rojos, plasma fresco congelado y se suspende la anticoagulación. Se procede a la realización de estudio endoscópico:
Videoendoscopía digestiva alta: (día 12): Esófago: cambio mucoso a 40 cm del ADS. Se observan cordones varicosos que desaparecen con la insuflación. A nivel de cambio mucoso, en hora 5, se observa una erosión menor de 5 mm.
Estómago: abundante edema de mucosa gástrica que distorsiona la normal anatomía y dificulta la correcta insuflación de la cavidad gástrica. A nivel de curvatura menor se observa una lesión ulcerosa de unos 20 mm, con fondo fibrinoso y edema perilesional.
Duodeno: duodenitis erosiva.
Conclusión: Esofagitis grado A. Várices esofágicas grado I. Ulcera gástrica Forrest III. Abundante edema gástrico (Imagen 9).
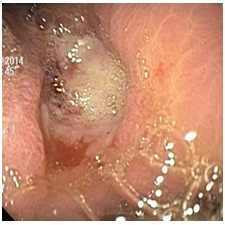
Imagen 9: Videoendoscopia digestiva alta: Se observa úlcera gástrica Forrest III. Abundante edema gástrico.
El paciente evoluciona estable hemodinámicamente. Sin nuevos signos de sangrado. Por lo que se continúa con su estudio.
Cistoscopia (día 18): Se observa mucosa de aspecto normal. Se obtienen muestras para biopsia sin alteraciones al examen anatomopatológico.
Colonoscopia virtual (día 19): Se observa engrosamiento parietal circunferencial, difuso del recto, en su unión con colon sigmoides que presenta escasa distensión en posición prono.
Engrosamiento difuso de la pared posterior y lateral de la vejiga.
Videocolonoscopia: (día 21): A 20 cm del margen anal se observa zona de retracción e imagen de compresión extrínseca (recto superior) (Imagen 10). Hemorroides internas.
Imagen 10:
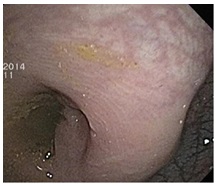
Imagen 10: Videocolonoscopia: Se observa zona de retracción e imagen de compresión extrínseca en recto superior.
 Presentación: Dra. Pamela Dip (1).
Presentación: Dra. Pamela Dip (1).
Discusión: Dr. Matías Cúneo (1).
Anatomía Patológica: Dr. Martín Mondino (2). Dra. Susana Marquez (2), Dra. Ana Lía Nocito (2).
1) Primera Cátedra de Clínica Médica. Facultad de Ciencias Médicas. Universidad Nacional de Rosario; Servicio de Clínica Médica. Hospital provincial Centenario. Rosario. Santa Fe. Argentina. 2) Cátedra de Anatomía y Fisiología Patológica. Facultad de Ciencias Médicas. Universidad Nacional de Rosario.
3º Parte: Discusión y resolución:
Discusión del caso clínico:
Estamos frente al caso de un paciente varón de 58 años sin antecedentes de jerarquía, que consulta por cuadro de un mes de evolución caracterizado por dolor y distensión abdominal, hiporexia, nauseas, vómitos y pérdida de peso. Presentando al ingreso insuficiencia renal, ascitis y sospecha, por imágenes compatibles, de fibrosis retroperitoneal.
Objetivos:
• Replantear el diagnóstico de fibrosis retroperitoneal. Evaluar sus probables causas, metodología diagnóstica y tratamiento.
• Evaluar manifestaciones de la hipertensión portal prehepática y su relación con la ascitis.
• Interpretar la trombosis venosa del eje espleno-porto- mesentérica, evaluar causas, metodología diagnóstica y tratamiento.
• Discutir la necesidad de tratamiento anticoagulante y su momento de inicio.
La fibrosis retroperitoneal es una rara enfermedad que se caracteriza por fibrosis de los tejidos retroperitoneales, con una incidencia 1 caso por 100000 habitantes, siendo más frecuente en el sexo masculino con una relación 2/1, presentándose generalmente entre la quinta y sexta década de la vida.
Según la etiología se pueden clasificar en idiopáticas, conocidas también como enfermedad de Albarran-Ormond quien fue el primero que describió la enfermedad en 1905, que suponen el 70 por ciento de las causas, y las secundarias.
Entre las secundarias encontramos múltiples causas, entre ellas:
Drogas: derivados ergotamínicos, metisergida, bromocriptina, betabloqueantes, metildopa, hidrazalasina y AINES; infecciones principalmente tuberculosis, histoplasmosis y actinomicosis; neoplasias como sarcomas, seminomas, cáncer de ovario, linfomas de hodking no hodking, cáncer de estómago, próstata y mama, entre otros; procedimientos quirúrgicos abdominales y radioterapia.
A su vez, existe relación entre esta entidad y enfermedades autoinmunes como tiroiditis, vasculitis de mediano y pequeños vasos, espondilitis anquilosante, LES, artritis reumatoidea, glomerulonefritis asociadas a ANCA, cirrosis biliar primaria y colangitis esclerosante primaria.
Las manifestaciones clínicas varían según la etapa de presentación. En una etapa inicial suele presentar síntomas inespecíficos caracterizados por dolor abdominal, lumbar que suelen acentuarse e incrementarse con el tiempo. Otros síntomas no específicos incluyen pérdida de peso, malestar general, anorexia, claudicación, edema y hematuria. Pueden presentar síntomas secundarios a la compresión de los árboles vasculares, caracterizado por trombosis venosa profunda secundaria a obstrucción de la vena cava o venas iliacas además de isquemia intestinal debida a la compresión de vasos mesentéricos.
En etapa avanzada se puede presentar obstrucción uretral progresiva que suele evolucionar a la oliguria y la falla renal obstructiva como puede evidenciarse en las imágenes de nuestro caso.
Las alteraciones analíticas se caracterizan por aumento de los reactantes de fase aguda VES y PCR, y en un 60 por ciento suelen presentar anticuerpos antinucleares positivos.
En cuanto al estudio por imágenes, la ecografía muestra inicialmente dilatación ureteral con una masa periaórtica.
La tomografía computada (TC) es el estudio de elección, permite visualizar el grado de fibrosis y para evaluar la presencia de adenopatías y tumores. Cuando la fibrosis es de causa idiopática suele observarse una placa homogénea que envuelve a los vasos abdominales y a los órganos retroperitoneales. Cuando la masa es de causa maligna, suele desplazar a la aorta hacia adelante (signo de la aorta flotante) alejándola de la columna vertebral y lateralizar los uréteres.
Con respecto a la realización de biopsia en casos de sospecha de fibrosis retroperitoneal, no hay indicaciones precisas de su realización para confirmar el diagnóstico o descartar malignidad. Solo sería obligatoria si la localización de la masa es atípica, si la clínica o hallazgos radiológicos sugieren la presencia de una neoplasia o infección subyacente, o bien, si no presenta buena respuesta al tratamiento médico instaurado.
Nuestro paciente presenta manifestaciones clínicas compatibles con cuadros de fibrosis retroperitoneal en etapas avanzadas, presentando imágenes compatibles por medio de tomografía por lo cual considero a la fibrosis peritoneal como diagnóstico probable. La etiología de la misma fue considerada en primer lugar como idiopática, ya que presenta alteraciones analíticas caracterizada por leve aumentos de los reactantes de fase aguda, presenta imágenes compatible con lesiones de causa idiopática, no hay evidencia clínica, analítica e imagenológica de causas tumorales o infecciosas, no tiene antecedentes quirúrgicos abdominales o retroperitoneales y no consume ni consumió fármacos que puedan desarrollar este tipo de patología. En primera instancia la biopsia retroperitoneal estaría desaconsejada ya que no presenta evidencia clínica, analítica e imagenológica de un proceso infeccioso o neoplásico alguno.
Respecto a tratamiento, tiene 3 objetivos:
• Disminuir la obstrucción
• Detener el proceso fibrótico
• Evitar recaídas/recidivas
El pilar de tratamiento son los corticoides, considerándose que el 90% van a mejorar y su respuesta es relativamente rápida (semanas). Al ser una enfermedad poco frecuente no existen muchos trabajos y por lo tanto buen nivel de evidencia acerca de con qué tratar y cuánto tiempo.
Se recomienda el tratamiento con corticoides a dosis inmunosupresora por un periodo de tiempo de 8 meses. En caso de no presentar respuesta al tratamiento médico inicial se puede realizar tratamiento médico con corticoides e inmunosupresores como mofetil micofenolato por un periodo de tiempo de 24 meses.
Finalizaría estudios imagenológicos, incluyendo videocolonoscopia y cistoscopia para descartar malignidad de dichos sitios.
Sabemos que la hipertensión portal se define por un gradiente de presión venosa hepática (GPVH) mayor de 5 mmHg. Generalmente es causada por un aumento en la resistencia en el lecho vascular porta-hepático debido a la obstrucción al flujo, que está relacionada con la cirrosis en la gran mayoría de los pacientes. Sin embargo, una variedad de trastornos pueden causar hipertensión portal en ausencia de cirrosis, una condición conocida como "hipertensión portal no cirrótica."
La hipertensión portal se ha categorizado como prehepática, intrahepática, o poshepática basado en el sitio de la obstrucción al flujo sanguíneo. Las causas de la hipertensión portal intrahepática se han subdividido adicionalmente como presinusoidal, sinusoidal, o postsinusoidal sobre la base de la ubicación de la obstrucción del flujo de sangre portal en el hígado. La hipertensión portal presinusoidal es causada por la obstrucción al flujo a través del sistema venoso portal en la porción extrahepática de la vena porta (hipertensión portal extrahepática presinusoidal) o en el nivel de ramificaciones de la vena porta en el hígado (hipertensión portal intrahepática presinusoidal).
La etiología de la misma no está bien definida. Las causas que se asocian suelen ser estados de hipercoaguladibilidad por déficit del factor v de Leiden, déficit de proteína C, hiperhomocisteinemia, pancreatitis, hepatocarcinoma, cirrosis, síndrome mieloproliferativos, fibrosis retroperitoneal.
Las manifestaciones clínicas se pueden presentar mediante varices esofágicas o gástricas generalmente cuando la trombosis portal es crónica.
La esplenomegalia se presenta en el 50 por ciento de los pacientes con trombosis portal crónica.
La ascitis puede estar presente en aproximadamente el 10 por ciento de los pacientes, particularmente después de la hemorragia gastrointestinal en el que la reanimación con líquidos masiva puede conducir a hipoalbuminemia dilucional aguda.
Con respecto a las alteraciones analíticas hepáticas no suelen presentar grandes alteraciones.
Retomando el caso de nuestro paciente, presenta causa claras de hipertensión portal de causa prehepatica producida por la trombosis portal secundaria a la fibrosis retroperitoneal. Quedando alejadas las causas de hipertensión portal de causa sinusoidal o postsinusoidal considerando que el paciente no tiene antecedentes de consumo alcohol, presenta serologías virales para virus hepatitis B y C negativas y no presenta alteraciones analíticas en el hepatograma ni evidencia imagenológicas de hepatopatía crónica.
El tratamiento médico, incluye medidas higiénico-dietéticas, tratamiento con betabloqueantes para prevenir el sangrado variceal y protección gástrica. El tratamiento anticoagulante será desarrollado más adelante.
La trombosis venosa del eje espleno-porto mesentérico es una entidad de muy baja frecuencia, responsable del 5 a 10 % de la isquemia mesentérica aguda, presentando entre sus complicaciones más frecuentes la isquemia e infarto intestinal.
Las causas de trombosis venosa mesentérica se deben, a estados de hipercoagulabilidad, hipertensión portal, infecciones abdominales, traumatismos abdominales cerrados, pancreatitis, esplenectomía, tumores malignos, fibrosis retroperitoneal. Entre las manifestaciones clínicas, suele presentar una clínica subaguda caracterizada por dolor abdominal, nauseas, vómitos, hiporexia y pérdida de peso y una clínica aguda caracterizada por sangrado digestivos, inestabilidad hemodinámica y traslocación bacteriana. El diagnóstico imagenológico se puede realizar mediante TC abdominal con contraste, con una sensibilidad del 90%, permitiendo ver imágenes con engrosamiento mucoso intestinal y falta de relleno a nivel vascular.
Volviendo al caso clínico, nuestro paciente tiene una causa evidente de trombosis venosa mesentérica dado por la fibrosis retroperitoneal, y a su vez presenta una clínica de característica subaguda. A nivel tomográfico se constatan imágenes de falta de relleno vascular. Considero apropiado el diagnóstico de trombosis venosa mesentérica secundaria a la fibrosis retroperitoneal.
El tratamiento de la trombosis venosa mesentérica y del eje espleno portal según guías de tratamiento anticoagulante, se recomiendan realizar tratamiento lo más precoz posible. La recomendación de la anticoagulación se basa en que la observación de la recanalización espontanea es casi nula. En contraste una canalización parcial o completa se observa en un 40% de los casos. El objetivo de la recanalización es evitar el desarrollo de hipertensión portal y sus complicaciones entre ellas isquemia e infarto intestinal y TEP.
Se debe realizar tratamiento anticoagulante con heparina sódica o heparina de bajo peso molecular por un tiempo de 3 semanas con posterior anticoagulación vía oral por un tiempo de 4 a 6 meses. Se recomienda evaluar nuevamente con imágenes para observar la presencia de recanalización.
Ahora, en nuestro paciente que tuvo hemorragia digestiva alta, ¿Es seguro realizar tratamiento anticoagulante?
Las contraindicaciones al tratamiento anticoagulante se pueden clasificar en dos grandes grupos:
Se consideran contraindicaciones absolutas aquellas en la cuales no se debe anticoagular por el grave riesgo hemorrágico existente o relativas aquellas situaciones en las cuales la anticoagulación va a depender, en cada paciente, de la balanza entre el riesgo tromboembólico y riesgo hemorrágico. En el caso de nuestro paciente presenta una causa clara que contraindica inicialmente continuar con la anticoagulación que fue el sangrado digestivo secundario a una ulcera gástrica Forrest 3, por lo que considero apropiado haber suspendido la anticoagulación posterior al sangrado intestinal.
¿Cuándo reanudar la anticoagulación?
No existen estudios que hablen de cuando reanudar la anticoagulación en los pacientes con trombosis del eje espleno-porto-mesentérico que han presentado sangrado gastrointestinal.
Un estudio reciente en realizado en febrero del 2014 por Qureshi et al. diseñado para investigar reinstauración de anticoagulación en pacientes con fibrilación auricular (FA) y sangrado gastrointestinal mayor. El mismo evaluó a 653 pacientes con FA en tratamiento con warfarina que habían presentado sangrado gastrointestinal. Se evaluó el reinicio de la anticoagulación a los 7, 30 y 60 días posteriores al sangrado concluyendo los investigadores que reiniciar luego de los 7 días se asoció con disminución de episodios de tromboembolismo y mortalidad sin un aumento significativo en sangrado gastrointestinal recurrente en comparación con el reinicio después de 30 o 60 días.
Por lo tanto, en nuestro caso, teniendo en cuenta que el sangrado gastrointestinal se debió a una ulcera Forrest 3 con bajo riesgo de resangrado, y de los beneficios de la realización de terapia anticoagulante en estos casos considero apropiado reanudar la anticoagulación a los siete días después del sangrado gastrointestinal con las medidas adecuadas para evitar el resangrado mediante inhibidores de bomba de protones.
Conclusiones:
Considero que la causa de fibrosis retroperitoneal sea idiopática, no realizaría biopsia inicialmente y comenzaría el tratamiento médico con corticoides.
La falla renal se interpretó de causa obstructiva secundaria a la fibrosis retroperitoneal, por lo que considero apropiado esperar la respuesta médica al tratamiento médico y si no responde a la misma, realizar la descompresión quirúrgica de la vía urinaria.
La trombosis del eje es pleno- porto- mesentérico la interpreto secundaria a la fibrosis retroperitoneal y reanudaría el tratamiento médico anticoagulante.
Con respecto a la hipertensión portal prehepática, la causa de la misma se debe a la trombosis del eje venoso secundaria a la fibrosis retroperitoneal, considerando a la ascitis secundaria a la expansión con cristaloides, en el contexto de la hemorragia digestiva.
Al descartarse proceso infeccioso asociado y sin evidencias de otra causa identificable del cuadro abdominal se comienza tratamiento con Prednisona 1 mg/Kg por diagnóstico presuntivo de fibrosis retroperitoneal.
El 12do día de internación presenta episodios de melena con caída del hematocrito. Se realiza transfusión de glóbulos rojos, plasma fresco congelado y se suspende la anticoagulación. Se procede a la realización de estudio endoscópico:
Videoendoscopía digestiva alta: (día 12): Esófago: cambio mucoso a 40 cm del ADS. Se observan cordones varicosos que desaparecen con la insuflación. A nivel de cambio mucoso, en hora 5, se observa una erosión menor de 5 mm.
Estómago: abundante edema de mucosa gástrica que distorsiona la normal anatomía y dificulta la correcta insuflación de la cavidad gástrica. A nivel de curvatura menor se observa una lesión ulcerosa de unos 20 mm, con fondo fibrinoso y edema perilesional.
Duodeno: duodenitis erosiva.
Conclusión: Esofagitis grado A. Várices esofágicas grado I. Ulcera gástrica Forrest III. Abundante edema gástrico (Imagen 9).

Imagen 9: Videoendoscopia digestiva alta: Se observa úlcera gástrica Forrest III. Abundante edema gástrico.
El paciente evoluciona estable hemodinámicamente. Sin nuevos signos de sangrado. Por lo que se continúa con su estudio.
Cistoscopia (día 18): Se observa mucosa de aspecto normal. Se obtienen muestras para biopsia sin alteraciones al examen anatomopatológico.
Colonoscopia virtual (día 19): Se observa engrosamiento parietal circunferencial, difuso del recto, en su unión con colon sigmoides que presenta escasa distensión en posición prono.
Engrosamiento difuso de la pared posterior y lateral de la vejiga.
Videocolonoscopia: (día 21): A 20 cm del margen anal se observa zona de retracción e imagen de compresión extrínseca (recto superior) (Imagen 10). Hemorroides internas.
Imagen 10:

Imagen 10: Videocolonoscopia: Se observa zona de retracción e imagen de compresión extrínseca en recto superior.
3º Parte: Discusión y resolución

Discusión: Dr. Matías Cúneo (1).
Anatomía Patológica: Dr. Martín Mondino (2). Dra. Susana Marquez (2), Dra. Ana Lía Nocito (2).
1) Primera Cátedra de Clínica Médica. Facultad de Ciencias Médicas. Universidad Nacional de Rosario; Servicio de Clínica Médica. Hospital provincial Centenario. Rosario. Santa Fe. Argentina. 2) Cátedra de Anatomía y Fisiología Patológica. Facultad de Ciencias Médicas. Universidad Nacional de Rosario.
3º Parte: Discusión y resolución:
Discusión del caso clínico:
Estamos frente al caso de un paciente varón de 58 años sin antecedentes de jerarquía, que consulta por cuadro de un mes de evolución caracterizado por dolor y distensión abdominal, hiporexia, nauseas, vómitos y pérdida de peso. Presentando al ingreso insuficiencia renal, ascitis y sospecha, por imágenes compatibles, de fibrosis retroperitoneal.
Objetivos:
• Replantear el diagnóstico de fibrosis retroperitoneal. Evaluar sus probables causas, metodología diagnóstica y tratamiento.
• Evaluar manifestaciones de la hipertensión portal prehepática y su relación con la ascitis.
• Interpretar la trombosis venosa del eje espleno-porto- mesentérica, evaluar causas, metodología diagnóstica y tratamiento.
• Discutir la necesidad de tratamiento anticoagulante y su momento de inicio.
La fibrosis retroperitoneal es una rara enfermedad que se caracteriza por fibrosis de los tejidos retroperitoneales, con una incidencia 1 caso por 100000 habitantes, siendo más frecuente en el sexo masculino con una relación 2/1, presentándose generalmente entre la quinta y sexta década de la vida.
Según la etiología se pueden clasificar en idiopáticas, conocidas también como enfermedad de Albarran-Ormond quien fue el primero que describió la enfermedad en 1905, que suponen el 70 por ciento de las causas, y las secundarias.
Entre las secundarias encontramos múltiples causas, entre ellas:
Drogas: derivados ergotamínicos, metisergida, bromocriptina, betabloqueantes, metildopa, hidrazalasina y AINES; infecciones principalmente tuberculosis, histoplasmosis y actinomicosis; neoplasias como sarcomas, seminomas, cáncer de ovario, linfomas de hodking no hodking, cáncer de estómago, próstata y mama, entre otros; procedimientos quirúrgicos abdominales y radioterapia.
A su vez, existe relación entre esta entidad y enfermedades autoinmunes como tiroiditis, vasculitis de mediano y pequeños vasos, espondilitis anquilosante, LES, artritis reumatoidea, glomerulonefritis asociadas a ANCA, cirrosis biliar primaria y colangitis esclerosante primaria.
Las manifestaciones clínicas varían según la etapa de presentación. En una etapa inicial suele presentar síntomas inespecíficos caracterizados por dolor abdominal, lumbar que suelen acentuarse e incrementarse con el tiempo. Otros síntomas no específicos incluyen pérdida de peso, malestar general, anorexia, claudicación, edema y hematuria. Pueden presentar síntomas secundarios a la compresión de los árboles vasculares, caracterizado por trombosis venosa profunda secundaria a obstrucción de la vena cava o venas iliacas además de isquemia intestinal debida a la compresión de vasos mesentéricos.
En etapa avanzada se puede presentar obstrucción uretral progresiva que suele evolucionar a la oliguria y la falla renal obstructiva como puede evidenciarse en las imágenes de nuestro caso.
Las alteraciones analíticas se caracterizan por aumento de los reactantes de fase aguda VES y PCR, y en un 60 por ciento suelen presentar anticuerpos antinucleares positivos.
En cuanto al estudio por imágenes, la ecografía muestra inicialmente dilatación ureteral con una masa periaórtica.
La tomografía computada (TC) es el estudio de elección, permite visualizar el grado de fibrosis y para evaluar la presencia de adenopatías y tumores. Cuando la fibrosis es de causa idiopática suele observarse una placa homogénea que envuelve a los vasos abdominales y a los órganos retroperitoneales. Cuando la masa es de causa maligna, suele desplazar a la aorta hacia adelante (signo de la aorta flotante) alejándola de la columna vertebral y lateralizar los uréteres.
Con respecto a la realización de biopsia en casos de sospecha de fibrosis retroperitoneal, no hay indicaciones precisas de su realización para confirmar el diagnóstico o descartar malignidad. Solo sería obligatoria si la localización de la masa es atípica, si la clínica o hallazgos radiológicos sugieren la presencia de una neoplasia o infección subyacente, o bien, si no presenta buena respuesta al tratamiento médico instaurado.
Nuestro paciente presenta manifestaciones clínicas compatibles con cuadros de fibrosis retroperitoneal en etapas avanzadas, presentando imágenes compatibles por medio de tomografía por lo cual considero a la fibrosis peritoneal como diagnóstico probable. La etiología de la misma fue considerada en primer lugar como idiopática, ya que presenta alteraciones analíticas caracterizada por leve aumentos de los reactantes de fase aguda, presenta imágenes compatible con lesiones de causa idiopática, no hay evidencia clínica, analítica e imagenológica de causas tumorales o infecciosas, no tiene antecedentes quirúrgicos abdominales o retroperitoneales y no consume ni consumió fármacos que puedan desarrollar este tipo de patología. En primera instancia la biopsia retroperitoneal estaría desaconsejada ya que no presenta evidencia clínica, analítica e imagenológica de un proceso infeccioso o neoplásico alguno.
Respecto a tratamiento, tiene 3 objetivos:
• Disminuir la obstrucción
• Detener el proceso fibrótico
• Evitar recaídas/recidivas
El pilar de tratamiento son los corticoides, considerándose que el 90% van a mejorar y su respuesta es relativamente rápida (semanas). Al ser una enfermedad poco frecuente no existen muchos trabajos y por lo tanto buen nivel de evidencia acerca de con qué tratar y cuánto tiempo.
Se recomienda el tratamiento con corticoides a dosis inmunosupresora por un periodo de tiempo de 8 meses. En caso de no presentar respuesta al tratamiento médico inicial se puede realizar tratamiento médico con corticoides e inmunosupresores como mofetil micofenolato por un periodo de tiempo de 24 meses.
Finalizaría estudios imagenológicos, incluyendo videocolonoscopia y cistoscopia para descartar malignidad de dichos sitios.
Sabemos que la hipertensión portal se define por un gradiente de presión venosa hepática (GPVH) mayor de 5 mmHg. Generalmente es causada por un aumento en la resistencia en el lecho vascular porta-hepático debido a la obstrucción al flujo, que está relacionada con la cirrosis en la gran mayoría de los pacientes. Sin embargo, una variedad de trastornos pueden causar hipertensión portal en ausencia de cirrosis, una condición conocida como "hipertensión portal no cirrótica."
La hipertensión portal se ha categorizado como prehepática, intrahepática, o poshepática basado en el sitio de la obstrucción al flujo sanguíneo. Las causas de la hipertensión portal intrahepática se han subdividido adicionalmente como presinusoidal, sinusoidal, o postsinusoidal sobre la base de la ubicación de la obstrucción del flujo de sangre portal en el hígado. La hipertensión portal presinusoidal es causada por la obstrucción al flujo a través del sistema venoso portal en la porción extrahepática de la vena porta (hipertensión portal extrahepática presinusoidal) o en el nivel de ramificaciones de la vena porta en el hígado (hipertensión portal intrahepática presinusoidal).
La etiología de la misma no está bien definida. Las causas que se asocian suelen ser estados de hipercoaguladibilidad por déficit del factor v de Leiden, déficit de proteína C, hiperhomocisteinemia, pancreatitis, hepatocarcinoma, cirrosis, síndrome mieloproliferativos, fibrosis retroperitoneal.
Las manifestaciones clínicas se pueden presentar mediante varices esofágicas o gástricas generalmente cuando la trombosis portal es crónica.
La esplenomegalia se presenta en el 50 por ciento de los pacientes con trombosis portal crónica.
La ascitis puede estar presente en aproximadamente el 10 por ciento de los pacientes, particularmente después de la hemorragia gastrointestinal en el que la reanimación con líquidos masiva puede conducir a hipoalbuminemia dilucional aguda.
Con respecto a las alteraciones analíticas hepáticas no suelen presentar grandes alteraciones.
Retomando el caso de nuestro paciente, presenta causa claras de hipertensión portal de causa prehepatica producida por la trombosis portal secundaria a la fibrosis retroperitoneal. Quedando alejadas las causas de hipertensión portal de causa sinusoidal o postsinusoidal considerando que el paciente no tiene antecedentes de consumo alcohol, presenta serologías virales para virus hepatitis B y C negativas y no presenta alteraciones analíticas en el hepatograma ni evidencia imagenológicas de hepatopatía crónica.
El tratamiento médico, incluye medidas higiénico-dietéticas, tratamiento con betabloqueantes para prevenir el sangrado variceal y protección gástrica. El tratamiento anticoagulante será desarrollado más adelante.
La trombosis venosa del eje espleno-porto mesentérico es una entidad de muy baja frecuencia, responsable del 5 a 10 % de la isquemia mesentérica aguda, presentando entre sus complicaciones más frecuentes la isquemia e infarto intestinal.
Las causas de trombosis venosa mesentérica se deben, a estados de hipercoagulabilidad, hipertensión portal, infecciones abdominales, traumatismos abdominales cerrados, pancreatitis, esplenectomía, tumores malignos, fibrosis retroperitoneal. Entre las manifestaciones clínicas, suele presentar una clínica subaguda caracterizada por dolor abdominal, nauseas, vómitos, hiporexia y pérdida de peso y una clínica aguda caracterizada por sangrado digestivos, inestabilidad hemodinámica y traslocación bacteriana. El diagnóstico imagenológico se puede realizar mediante TC abdominal con contraste, con una sensibilidad del 90%, permitiendo ver imágenes con engrosamiento mucoso intestinal y falta de relleno a nivel vascular.
Volviendo al caso clínico, nuestro paciente tiene una causa evidente de trombosis venosa mesentérica dado por la fibrosis retroperitoneal, y a su vez presenta una clínica de característica subaguda. A nivel tomográfico se constatan imágenes de falta de relleno vascular. Considero apropiado el diagnóstico de trombosis venosa mesentérica secundaria a la fibrosis retroperitoneal.
El tratamiento de la trombosis venosa mesentérica y del eje espleno portal según guías de tratamiento anticoagulante, se recomiendan realizar tratamiento lo más precoz posible. La recomendación de la anticoagulación se basa en que la observación de la recanalización espontanea es casi nula. En contraste una canalización parcial o completa se observa en un 40% de los casos. El objetivo de la recanalización es evitar el desarrollo de hipertensión portal y sus complicaciones entre ellas isquemia e infarto intestinal y TEP.
Se debe realizar tratamiento anticoagulante con heparina sódica o heparina de bajo peso molecular por un tiempo de 3 semanas con posterior anticoagulación vía oral por un tiempo de 4 a 6 meses. Se recomienda evaluar nuevamente con imágenes para observar la presencia de recanalización.
Ahora, en nuestro paciente que tuvo hemorragia digestiva alta, ¿Es seguro realizar tratamiento anticoagulante?
Las contraindicaciones al tratamiento anticoagulante se pueden clasificar en dos grandes grupos:
Se consideran contraindicaciones absolutas aquellas en la cuales no se debe anticoagular por el grave riesgo hemorrágico existente o relativas aquellas situaciones en las cuales la anticoagulación va a depender, en cada paciente, de la balanza entre el riesgo tromboembólico y riesgo hemorrágico. En el caso de nuestro paciente presenta una causa clara que contraindica inicialmente continuar con la anticoagulación que fue el sangrado digestivo secundario a una ulcera gástrica Forrest 3, por lo que considero apropiado haber suspendido la anticoagulación posterior al sangrado intestinal.
¿Cuándo reanudar la anticoagulación?
No existen estudios que hablen de cuando reanudar la anticoagulación en los pacientes con trombosis del eje espleno-porto-mesentérico que han presentado sangrado gastrointestinal.
Un estudio reciente en realizado en febrero del 2014 por Qureshi et al. diseñado para investigar reinstauración de anticoagulación en pacientes con fibrilación auricular (FA) y sangrado gastrointestinal mayor. El mismo evaluó a 653 pacientes con FA en tratamiento con warfarina que habían presentado sangrado gastrointestinal. Se evaluó el reinicio de la anticoagulación a los 7, 30 y 60 días posteriores al sangrado concluyendo los investigadores que reiniciar luego de los 7 días se asoció con disminución de episodios de tromboembolismo y mortalidad sin un aumento significativo en sangrado gastrointestinal recurrente en comparación con el reinicio después de 30 o 60 días.
Por lo tanto, en nuestro caso, teniendo en cuenta que el sangrado gastrointestinal se debió a una ulcera Forrest 3 con bajo riesgo de resangrado, y de los beneficios de la realización de terapia anticoagulante en estos casos considero apropiado reanudar la anticoagulación a los siete días después del sangrado gastrointestinal con las medidas adecuadas para evitar el resangrado mediante inhibidores de bomba de protones.
Conclusiones:
Considero que la causa de fibrosis retroperitoneal sea idiopática, no realizaría biopsia inicialmente y comenzaría el tratamiento médico con corticoides.
La falla renal se interpretó de causa obstructiva secundaria a la fibrosis retroperitoneal, por lo que considero apropiado esperar la respuesta médica al tratamiento médico y si no responde a la misma, realizar la descompresión quirúrgica de la vía urinaria.
La trombosis del eje es pleno- porto- mesentérico la interpreto secundaria a la fibrosis retroperitoneal y reanudaría el tratamiento médico anticoagulante.
Con respecto a la hipertensión portal prehepática, la causa de la misma se debe a la trombosis del eje venoso secundaria a la fibrosis retroperitoneal, considerando a la ascitis secundaria a la expansión con cristaloides, en el contexto de la hemorragia digestiva.